


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
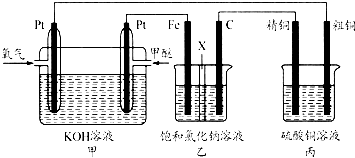
查看答案和解析>>
科目:高中化学 来源: 题型:

| 体系pH | 不同温度下NaBH4的半衰期(min) | |||
| 0℃ | 25℃ | 50℃ | 75℃ | |
| 8 | 4.32×100 | 6.19×10-1 | 8.64×10-2 | 1.22×10-2 |
| 10 | 4.32×102 | 6.19×101 | 8.64×100 | 1.22×100 |
| 12 | 4.32×104 | 6.19×103 | 8.64×102 | 1.22×102 |
| 14 | 4.32×106 | 6.19×105 | 8.64×104 | 1.22×104 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液因不带电而稳定,胶体因带电而不稳定 |
| B、做焰色反应实验前,铂丝应先用盐酸洗涤后灼烧至无色 |
| C、氯水与亚硫酸钠溶液的混合液,漂白性更强 |
| D、不慎将浓硫酸沾到皮肤上,立即用大量水冲洗,然后涂上烧碱溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 |
| 化学式 | ①HCl ② | ③ ④Ba(OH)2 | ⑤Na2CO3 ⑥ | ⑦CO2 ⑧Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
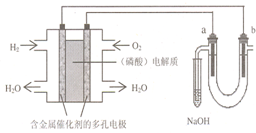 用酸性氢氧燃料电池电解苦卤水 (含Cl-、Br-、Na+、Mg2+)的装置如图所示 (a、b为石墨电极).下列说法中,正确的是( )
用酸性氢氧燃料电池电解苦卤水 (含Cl-、Br-、Na+、Mg2+)的装置如图所示 (a、b为石墨电极).下列说法中,正确的是( )| A、电池工作时,负极反应式为:H2+2 OH--2e-=2H2O |
| B、电解时,a 电极周围首先放电的是Br-而不是Cl-,说明当其它条件相同时前者的还原性强于后者 |
| C、电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极 |
| D、忽略能量损耗,当电池中消耗0.32g O2时,b 极周围会产生0.04g H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该温度下,0.01 mol?L-1醋酸溶液的pH=4 |
| B、该温度下,用0.1 mol?L-1醋酸和0.01 mol/L醋酸分别完全中和等体积0.1 mol?L-1的NaOH溶液,消耗两醋酸的体积比为1:10 |
| C、该温度下,0.2 mol?L-1醋酸溶液和0.4 mol?L-1醋酸钠溶液等体积混合后,混合液的pH<4.7 |
| D、该温度下,0.2 mol?L-1盐酸溶液和0.4 mol?L-1醋酸钠溶液等体积混合后,混合液的pH>4.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 的质量分数,在实验室中按以下步骤进行实验:
的质量分数,在实验室中按以下步骤进行实验:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应中氧化剂与还原剂的物质的量比值为3:2 |
| B、反应中NaOH既不是氧化剂也不是还原剂 |
| C、当有0.2mol Fe(OH)3参加反应时转移的电子数目为1.204×1023 |
| D、反应中NaClO被还原,发生还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com