
| A. | D2+>B2+>A2+>C2+ | B. | A2+>B2+>C2+>D2+ | C. | C2+>A2+>B2+>D2+ | D. | A2+>C2+>D2+>B2+ |
分析 一般来说,作原电池负极的金属活动性较大,活泼金属能将较不活泼金属从其盐溶液中置换出来,据此判断金属的活动性强弱以及离子的氧化性强弱.
解答 解:一般来说,作原电池负极的金属活动性较大,活泼金属能将较不活泼金属从其盐溶液中置换出来,将A、B用导线连接后浸在稀硫酸中,A上放出氢气,B逐渐溶解生成B2+,B溶解作负极,则活泼性强弱B>A,金属阳离子的氧化性A2+>B2+;在含 A2+和C2+的混合溶液中加入铁,铁棒先析出C,则金属活泼性强弱A>C,金属阳离子的氧化性C2+>A2+;把D放入B的硝酸盐溶液中,则D表面有B析出,则金属活泼性D>B,金属阳离子的氧化性B2+>D2+,据分析知,四种金属阳离子的氧化性由强到弱的顺序是C2+>A2+>B2+>D2+,
故选C.
点评 本题考查金属活动性顺序强弱判断,侧重考查知识运用能力,明确原电池中正负极与金属活泼性的关系、金属之间的置换反应即可解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 水中,c(H+)•c(OH-)=1×10-14 | |
| B. | 纯水或水溶液中25℃时,c(H+)•c(OH-)=1×10-14 | |
| C. | NaOH溶液在25℃时,c(H+)•c(OH-)>1×10-14 | |
| D. | 溶液浓度改变或酸碱度改变,Kw随之改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯是无色且带有特殊气味的液体 | |
| B. | 常温下苯是一种不溶于水且密度小于水的液体 | |
| C. | 苯在一定条件下能与溴发生取代反应 | |
| D. | 苯分子中不含碳碳双键,不可能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每生成1mol Fe3O4,反应转移的电子总数为3mol | |
| B. | Fe2+和S2O32-都是还原剂 | |
| C. | 1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为$\frac{1}{3}$mol | |
| D. | x=6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯的最简式:C6H6 | B. | 乙烯分子的结构简式为:CH2CH2 | ||
| C. | 一氯甲烷的电子式为: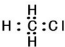 | D. | 2-甲基丁烷的键线式: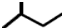 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H1>△H2>△H3 | B. | △H2<△H1<△H3 | C. | △H1=△H2=△H3 | D. | △H1>△H3>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com