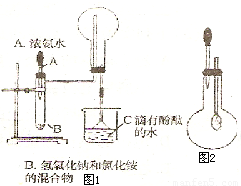
I.如图1是某学生设计的制取和收集某些气体的实验装置(可加热).

(1)该装置在加入反应物前,应首先进行的实验操作是
检查装置气密性
检查装置气密性
.
(2)下列气体的制取中,若用排空气法收集,可使用该装置制备和收集的是(选填编号,下同)
①③
①③
若用排水法收集(集气瓶中充满水),可使用该装置制备和收集的是
①④⑤
①④⑤
.
①用Zn与稀盐酸反应制H
2②用CaCO
3与稀盐酸反应制CO
2③用固体NaOH和浓氨水制NH
3④用Cu与稀HNO
3反应制NO
⑤用MnO
2与双氧水反应制O
2⑥浓硫酸与铜片反应制SO
2⑦用MnO
2与浓盐酸反应制Cl
2II.某校化学研究性学习小组对浓硫酸与金属锌的反应进行探究.首先按图2组装好实验装置,然后取一定量的浓硫酸与足量Zn充分反应,微热试管A,实验过程中先观察到C、D中均有气泡产生,D中开始出现浑浊,后浑浊消失,随后气泡量逐渐减少,品红溶液褪色,反应较长时间后,C、D中的气泡量又会明显增加.
试回答:
(1)从甲、乙中选择合适的装置填入B、C中,并进行正确连接,a接
3或4
3或4
、
4或3
4或3
接b,c接
1
1
、
2
2
接d;
(2)D、E试管中CCl
4溶液的作用是防止溶液倒吸,该实验中起到同样作用的装置是
乙
乙
;
(3)能证明浓硫酸具有强氧化性的实验现象为
C中品红溶液褪色
C中品红溶液褪色
;
(4)反应较长时间后气泡量又会明显增加的原因是
浓H2SO4变成稀H2SO4,与Zn反应放出H2
浓H2SO4变成稀H2SO4,与Zn反应放出H2
;
(5)D中浑浊消失的离子方程式为
SO2+CaSO3+H2O=Ca2++2HSO3-
SO2+CaSO3+H2O=Ca2++2HSO3-
.

 如图1和2是某校实验探究小组制备NH3 并进行性质实验时的改进装置.按图1把仪器安装好,称取2g 固体氯化铵装入试管底部,再快速称取2g 氢氧化锅覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸人约2mL浓氨水);烧杯内盛滴有酚酞试液的水.把浓氨水滴人试管里,可立即观察到试管内发生剧烈反应,有大量气泡产生.将上述装置中收满NH3的圆底烧瓶取下,改装成图2所示的装置,胶头滴管内事先吸人2mLH2O,此时小气球系在玻璃管上呈自然松驰状态;将滴管内的水慢慢滴人烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某个性质.按要求回答下列问题:
如图1和2是某校实验探究小组制备NH3 并进行性质实验时的改进装置.按图1把仪器安装好,称取2g 固体氯化铵装入试管底部,再快速称取2g 氢氧化锅覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸人约2mL浓氨水);烧杯内盛滴有酚酞试液的水.把浓氨水滴人试管里,可立即观察到试管内发生剧烈反应,有大量气泡产生.将上述装置中收满NH3的圆底烧瓶取下,改装成图2所示的装置,胶头滴管内事先吸人2mLH2O,此时小气球系在玻璃管上呈自然松驰状态;将滴管内的水慢慢滴人烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某个性质.按要求回答下列问题: NH3↑+H2O;⑤NH4Cl会分解释放出NH3.
NH3↑+H2O;⑤NH4Cl会分解释放出NH3. 2NH3↑+2H2O+CaCl2,
2NH3↑+2H2O+CaCl2, 2NH3↑+2H2O+CaCl2;
2NH3↑+2H2O+CaCl2; NH3↑+H2O;但该温度条件下,NH4Cl不会分解;
NH3↑+H2O;但该温度条件下,NH4Cl不会分解;

 阅读快车系列答案
阅读快车系列答案 如图1和2是某校实验探究小组制备NH3 并进行性质实验时的改进装置.按图1把仪器安装好,称取2g 固体氯化铵装入试管底部,再快速称取2g 氢氧化锅覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL浓氨水);烧杯内盛滴有酚酞试液的水.把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡产生.将上述装置中收满NH3的圆底烧瓶取下,改装成图2所示的装置,胶头滴管内事先吸入2mLH2O,此时小气球系在玻璃管上呈自然松驰状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某个性质.按要求回答下列问题:
如图1和2是某校实验探究小组制备NH3 并进行性质实验时的改进装置.按图1把仪器安装好,称取2g 固体氯化铵装入试管底部,再快速称取2g 氢氧化锅覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL浓氨水);烧杯内盛滴有酚酞试液的水.把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡产生.将上述装置中收满NH3的圆底烧瓶取下,改装成图2所示的装置,胶头滴管内事先吸入2mLH2O,此时小气球系在玻璃管上呈自然松驰状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某个性质.按要求回答下列问题:

 NH3↑+H2O;⑤NH4Cl会分解释放出NH3.
NH3↑+H2O;⑤NH4Cl会分解释放出NH3.