
| A. | 化学反应进行的越快,化学反应现象越明显 | |
| B. | 某反应中,经2min后B浓度减少0.6mol•L-1,在2min时用B表示的反应速率为0.6mol•L-1•min | |
| C. | 化学反应中的能量变化都是化学能转化成热能 | |
| D. | 原电池的反应一定是氧化还原反应 |
分析 A.有些反应无明显反应现象;
B.化学反应速率表示某一时间段内平均反应速率而不是即时反应速率;
C.化学反应中的能量变化可能是化学能转化为热能,可能是化学能转化为光能等;
D.只有自发进行的放热的氧化还原反应才能设计成原电池.
解答 解:A.有些反应无明显反应现象,如酸碱中和反应,故A错误;
B.化学反应速率表示某一时间段内平均反应速率而不是即时反应速率,所以某反应中,经2min后B浓度减少0.6mol•L-1,在2min内用B表示的反应速率为0.6mol/(L•min),故B错误;
C.化学反应中的能量变化可能是化学能转化为热能,可能是化学能转化为光能等,故C错误;
D.只有自发进行的放热的氧化还原反应才能设计成原电池,所以原电池的反应一定是氧化还原反应,故D正确;
故选D.
点评 本题考查反应速率的计算、能量变化、原电池反应特点等知识点,为高频考点,注意原电池反应必须特点,易错选项是B,题目难度不大.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCI和NaOH反应的中和热△H=-57.3kJ?mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ?mol-1 | |
| B. | 需要加热才能发生的反应一定是吸热反应 | |
| C. | CO(g)的燃烧热是283.0kJ?mol-1,则2CO2(g)═2CO(g)+O2(g)反应的△H=+2×283.0kJ?mol-1 | |
| D. | 1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲醇(CH3OH)和乙醇互为同系物 | |
| B. | 不同元素的原子构成的分子只能含极性共价键 | |
| C. | ${\;}_{92}^{235}$U和${\;}_{92}^{238}$U是中子数不同质子数相同的同种核素 | |
| D. | 短周期第IVA与VIIA族元素的原子间构成的分子,均不满足原子最外层8电子结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可以用分液漏斗分离硝基苯和苯 | |
| B. | 加浓溴水,然后过滤可以除去苯中少量乙烯 | |
| C. | 苯、溴水、铁粉混合制得溴苯 | |
| D. | 用溴水可以鉴别苯、乙醇、苯乙烯( ) ) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
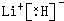 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸乙酯、甲苯、十一烷 | B. | 乙醇、苯、庚烯 | ||
| C. | 甘油、甲醛、硝基苯 | D. | 溴苯、四氯化碳、苯磺酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙溶于醋酸CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 锌片插入硝酸银溶液中Zn+Ag+═Zn2++Ag | |
| C. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++HCO3- | |
| D. | 硫酸镁溶液和氢氧化钡溶液反应 SO42-+Ba2+═BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com