
| A. | pH=2与pH=1的硝酸中c(H+)之比为1:10 | |
| B. | Na2CO3溶液中c(Na+)与c(CO32-)之比为2:1 | |
| C. | 0.2 mol•L-1与0.1mol/L醋酸中c (H+)之比为2:1 | |
| D. | NO2溶于水时,被氧化的n(NO2)与被还原的n(NO2)之比为3:1 |
分析 A.酸中c(H+)=10-pH;
B.碳酸钠是强碱弱酸盐,碳酸根离子水解;
C.醋酸是弱电解质,醋酸浓度越大其电离程度越小;
D.二氧化氮和水反应生成硝酸和NO,且硝酸和NO的物质的量之比是2:1,被氧化的二氧化氮占$\frac{2}{3}$,被还原的二氧化氮占$\frac{1}{3}$.
解答 解:A.酸中c(H+)=10-pH,所以pH=2与pH=1的硝酸中c(H+)之比=0.01mol/L:0.1mol/L=1:10,故A正确;
B.碳酸钠是强碱弱酸盐,碳酸根离子水解,所以c(Na+)与c(CO32-)之比大于2:1,故B错误;
C.醋酸是弱电解质,醋酸浓度越大其电离程度越小,所以0.2 mol•L-1与0.1mol/L醋酸中c(H+)之比小于2:1,故C错误;
D.二氧化氮和水反应生成硝酸和NO,且硝酸和NO的物质的量之比是2:1,被氧化的二氧化氮占$\frac{2}{3}$,被还原的二氧化氮占$\frac{1}{3}$,所以被氧化的n(NO2)与被还原的n(NO2)之比为2:1,故D错误;
故选A.
点评 本题考查盐类水解、pH的计算、氧化还原反应、弱电解质的电离等知识点,侧重考查学生分析计算能力,注意:弱电解质溶液浓度越小其电离程度越大,易错选项是C.


科目:高中化学 来源: 题型:解答题
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
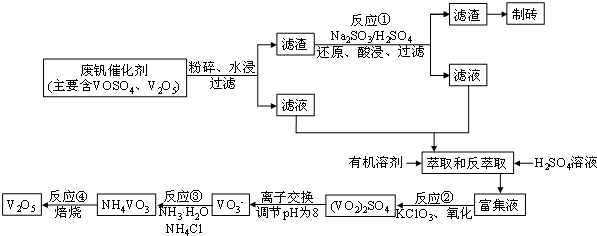
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上月考一化学卷(解析版) 题型:选择题
一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示。下列判断正确的是
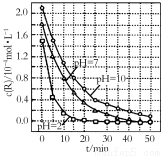
A.R的起始浓度越小,降解速率越大
B.在0~50 min之间,pH=2和pH=7时R的降解百分率相等
C.溶液酸性越 强,R的降解速率越小
强,R的降解速率越小
D.在20~25 min之间,pH=10时R的平均降解速率为0.04 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在转移液体前容量瓶中有少量蒸馏水 | |
| B. | 定容摇匀后,液面已低于容量瓶刻度线,此时再加水 | |
| C. | 转移时有少许液体沿容量瓶外壁流到实验桌上 | |
| D. | 定容时俯视液面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+ 1s22s22p63s23p6 | B. | O2-1s22s23p4 | ||
| C. | Cl- 1s22s22p63s23p6 | D. | Ar 1s22s22p63s23p6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验卤代烃中是否含有氯,可将其与NaOH溶液共热后滴加AgNO3溶液即可 | |
| B. | 根据外加电源的阴极保护法,把钢闸门与外加电源的正极连接就可以被保护 | |
| C. | 将乙醇与浓的氢溴酸混合加热可以制备溴乙烷 | |
| D. | 做过银镜反应实验的试管内壁附着银,用稀氨水可以洗去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ | |
| B. | 除去CO2中的SO2:SO2+CO32-═CO2↑+SO32- | |
| C. | 0.01 mol SO2气体通入10 mL 1 mol/L的NaOH溶液中:SO2+OH-═HSO3- | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu+稀HNO3 | B. | Cu$\stackrel{空气、△}{→}$CuO$\stackrel{硝酸}{→}$Cu(NO3)2 | ||
| C. | Cu+浓HNO3 | D. | Cu$\stackrel{Cl_{2}}{→}$CuCl2$\stackrel{AgNO_{3}}{→}$Cu(NO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
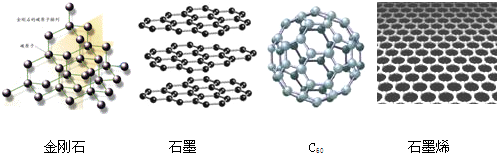
| A. | 金刚石和石墨烯中碳原子的杂化方式不同 | |
| B. | 金刚石、石墨、C60 和石墨烯的关系:互为同素异形体 | |
| C. | 这四种物质完全燃烧后的产物都是CO2 | |
| D. | 石墨与C60的晶体类型相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com