
| A. | 马口铁(锡铁)镀层破损后被腐蚀时,首先是镀层被氧化 | |
| B. | 原电池反应是导致金属腐蚀的主要原因,故不能用于减缓金属的腐蚀 | |
| C. | 钢铁电化学腐蚀的两种主要类型其主要区别在于水膜的pH不同引起负极反应的不同 | |
| D. | 无论哪种类型的金属腐蚀,其实质都是金属被氧化 |
分析 A、铁与锡在一起时,铁活泼易被腐蚀;
B、作原电池正极的金属被保护;
C、钢铁电化学腐蚀的两种类型主要区别在于水膜的pH不同,引起的正极反应不同;
D、金属被腐蚀实质是金属失电子.
解答 解:A、马口铁(镀锡铁)镀层破损后被腐蚀时,铁与锡在一起形成原电池,铁活泼作负极易被腐蚀,所以首先是铁被氧化,故A错误;
B、原电池反应是导致金属腐蚀的主要原因,但当金属做为正极时不会发生反应,故正极被保护,故B错误;
C、钢铁电化学腐蚀的两种类型主要区别在于水膜的PH不同,引起的正极反应不同,根据水膜的酸性的强弱,可以分为析氢腐蚀和吸氧腐蚀,故C错误;
D、金属被腐蚀实质是金属失电子,所以无论哪种类型的腐蚀,其实质都是金属被氧化,故D正确.
故选D.
点评 本题考查学生金属的腐蚀和防护知识,注意把握金属的腐蚀原理和防护方法,注意基本概念的理解和掌握是关键,难度不大.


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③④⑤ | C. | ④⑤⑥ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CsOH的碱性比KOH强 | B. | ${\;}_{55}^{137}$Cs中有82个中子 | ||
| C. | HI比HF还原性强 | D. | KIO3是碘的最高价含氧酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,23 g NO2和N2O4的混合气体中含有NA个氧原子 | |
| B. | 1 mol氯气与足量的氢氧化钠溶液反应电子转移总数为2NA | |
| C. | 500 mL1 mol•L-1 MgCl2溶液中含有Cl-数目为0.5NA | |
| D. | 标况下11.2 L H2O与4.0gCH4所含氢原子个数均为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
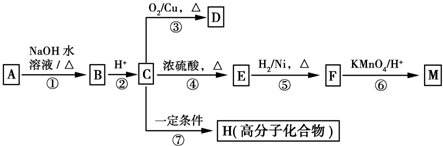
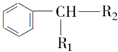 $→_{H+}^{KMnO_{4}}$
$→_{H+}^{KMnO_{4}}$ 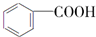 (R1、R2表示烃基或氢原子)
(R1、R2表示烃基或氢原子)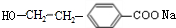 .
.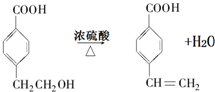 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
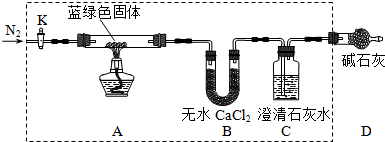
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑤⑧ | B. | ④⑤⑦⑧ | C. | ④⑤⑧ | D. | ③④⑤⑦⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com