



 CH3COOH+OH-
CH3COOH+OH- CH3COOH+OH-
CH3COOH+OH-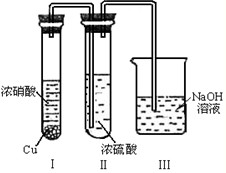
 ��CΪNa2O2��
��CΪNa2O2�� �� Na2O2��
�� Na2O2�� CH3COOH+OH-����Һ�ʼ��ԣ�pH��7��
CH3COOH+OH-����Һ�ʼ��ԣ�pH��7�� CH3COOH+OH-��
CH3COOH+OH-��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�





�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


| ||
| �� |
| ||
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
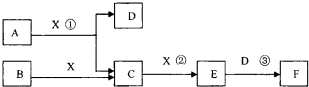
��15�֣������ڳ���Ԫ���γɵĴ�����A��B��C��D��Eת����ϵ����ͼ��ʾ������A������B֮��ķ�Ӧ������Һ�н��У�E������A��B���������е�ij����ͬ����
��ش��������⣺
��1����AΪ������C�����ӻ����D��һ��ǿ�д��A�����ӽṹʾ��ͼ ��C�Ļ�ѧʽ ��D������ʵ������ᷴӦ������Һ��PH____________7,(���������)��ԭ���ǣ������ֺ����ӷ���ʽ˵���� ��
��2����C��һ�����壬D��һ��ǿ�ᣬ��
��C��ˮ��Ӧ�Ļ�ѧ����ʽΪ ��
��������Ϊ��ŨH2SO4���Ը�������C����ijͬѧΪ����֤�ù۵��Ƿ���ȷ������ͼװ�ý���ʵ�顣ʵ������У�ŨH2SO4��δ�����������ݳ����ұ�Ϊ����ɫ������ó��Ľ����� ��
����֪������1 mol����C��H2O��Ӧ����D��Һ��E����ų�46kJ������д������C��H2O��Ӧ����D��Һ��E������Ȼ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com