
将4 mol A气体和2 mol B气体在2 L的密闭容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g);ΔH<0,4 s后反应达到平衡状态,此时测得C的浓度为0.6mol/L,下列说法中正确的是( )
2C(g);ΔH<0,4 s后反应达到平衡状态,此时测得C的浓度为0.6mol/L,下列说法中正确的是( )
A.反应过程中,当A、B、C的物质的量浓度之比为2∶1∶2时,反应即达到平衡状态
B.4 s内用物质B表示的反应速率为0.075 mol/(L·s)
C.达平衡后若增大压强,A的转化率降低
D.达平衡后若升高温度,平衡常数增大
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
工业废水中含有多种有害成分,任意排放将造成严重污染,进行分类处理达标后才能排放。
(1)含有Cu2+等离子的废水,常加入FeS等难溶物质作为沉淀剂除去。请用离子方程式说明上述除杂的原理 。实验室可利用FeS制取H2S,若将H2S通入足量NaOH溶液中,所得溶液中Na+与其他微粒的浓度关系是c(Na+)= 。
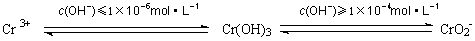 (2)含铬废水有毒,危害很大.处理方法是在含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去.用离子方程式表示溶液pH不能超过10的原因 。
(2)含铬废水有毒,危害很大.处理方法是在含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去.用离子方程式表示溶液pH不能超过10的原因 。
已知:
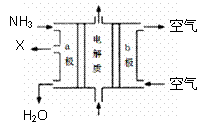 (3)废水中的氨可以回收再利用。
(3)废水中的氨可以回收再利用。
①氨能设计成如图所示的碱性燃料电池。产生的X气体可直接排放到大气中。a电极作 极,其电极反应式为
。
②加水稀释氨水的过程中,下列表达式的数值变大的是 。
A.c(H+) B.c(OH-)/c(NH3·H2O)
C.c(H+)·c(OH-) D.c(NH4+) +c(H+)
③T℃下, NH3·H2O的电离常数为Ka,NH4+的水解平衡常数为Kh,则该温度下水的离子积常数Kw= 。
④一定条件下,向某密闭容器中加入一定量的N2和H2发生可逆反应:
N2(g)+3H2(g) 2NH3(g)ΔH=-92.2 kJ·mol-1,测得0到10 s内,c(H2)减小了0.75 mol·L-1,下列说法正确的是( )
2NH3(g)ΔH=-92.2 kJ·mol-1,测得0到10 s内,c(H2)减小了0.75 mol·L-1,下列说法正确的是( )
A.该反应的逆反应的活化能不小于92.2 kJ·mol-1
B.10 s内氨气的平均反应速率为0.025 mol·L-1·s-1
C.10 s到15 s内c(NH3)增加量小于0.25 mol·L-1
D.达平衡后,分离出少量NH3,平衡向正反应方向移动,v正增大
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色透明溶液与铝反应放出氢气,该溶液中可能含有Mg2+、Cu2+、Ba2+、H+、Ag+、SO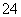 、SO
、SO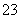 、HCO
、HCO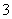 、OH-、NO
、OH-、NO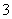 十种离子中的若干种,下列推断正确的是 ( )
十种离子中的若干种,下列推断正确的是 ( )
A.当溶液中有Al3+生成时,溶液中可能存在:SO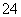 、NO
、NO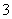 、H+、Mg2+
、H+、Mg2+
B.当溶液中有Al3+生成时,溶液中一定存在:H+、SO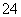 ;可能存在Mg2+
;可能存在Mg2+
C.当溶液中有[Al(OH)4]-生成时,溶液中一定存在:OH-、Ba2+、NO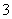
D.当溶液中有[Al(OH)4]-生成时,溶液中可能存在:OH-、Ba2+、NO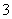 、SO
、SO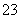
查看答案和解析>>
科目:高中化学 来源: 题型:
若化合物ABn的中心原子A上没有孤对电子,运用价层电子对互斥理论,下列说法正确的是( )
A.若n=2,则分子的立体结构为V形
B.若n=3,则分子的立体结构为三角锥形
C.若n=4,则分子的立体结构为正四面体形
D.以上说法都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定。
 (1)该实验应选用 作指示剂;
(1)该实验应选用 作指示剂;
(2)右图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的 刻度为25,滴定管中液面读数应为 mL;
(3)为了减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为c mo1/L,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.35 | 25.30 |
从上表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是 。
A.实验结束时俯视刻度线读取滴定终点时NaOH溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗,
E.滴加NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
(4)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不必化简):
C(CH3COOH)= mo1/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)工业制氢气的一个重要反应是:CO(g)+H2O(g) CO2(g)+ H2(g)
CO2(g)+ H2(g)
已知在25℃时:(1)C(石墨)+1/2O2(g)=CO(g) ΔH1=—111kJ/mol
(2)H2(g)+1/2O2(g)=H2O(g) ΔH2=—242kJ/mol
(3)C(石墨)+O2(g)=CO2(g) ΔH3=—394kJ/mol
试计算25℃时一氧化碳与水作用转化为氢气和二氧化碳反应的反应热 。
(2)已知上述反应在427℃ 时的平衡常数是9.4。如果反应开始时,一氧化碳和水蒸气的浓度都是0.01 mol/L,计算一氧化碳在此反应条件下的转化率 。(保留3位有效数字)。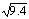 ≈3.07。
≈3.07。
(3)对于化学反应,速率也是研究的重要内容。在一密闭容器中充入1mol H2和1mol I2,压强为p(Pa) ,并在一定温度下使其发生反应:H2(g)+I2(g)  2HI(g) ΔH<0。达到平衡后,以下能加快反应速率的是( )
2HI(g) ΔH<0。达到平衡后,以下能加快反应速率的是( )
①保持容器容积不变,向其中加入1mol H2。
②保持容器容积不变,向其中加入1mol N2(N2不参加反应)。
③保持容器内气体压强不变,向其中加入1mol N2(N2不参加反应)。
④保持容器内气体压强不变,向其中加入1mol H2和1mol I2。
⑤提高起始的反应温度。
(4)2.0 mol PCl3和1.0molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应:
PCl3(g)+ Cl2(g) PCl5(g)。达平衡时,PCl5为0.40mol,如果此时移走1.0 mol PCl3和0.5molCl2,在相同温度下再达平衡时PCl5的物质的量是( )
PCl5(g)。达平衡时,PCl5为0.40mol,如果此时移走1.0 mol PCl3和0.5molCl2,在相同温度下再达平衡时PCl5的物质的量是( )
A.0.4 mol B.0.2 mol C.小于0.2 mol D.大于0.2 mol,小于0.4 mol
(5)已知25℃下,醋酸溶液中存在下述关系: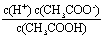 =1.75×10-5其中的数值是该温度下醋酸的电离平衡常数。若醋酸的起始浓度为0.010 mol/L,平衡时c(H+)= . (
=1.75×10-5其中的数值是该温度下醋酸的电离平衡常数。若醋酸的起始浓度为0.010 mol/L,平衡时c(H+)= . (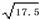 ≈4.18)
≈4.18)
(提示:醋酸的电离常数很小,平衡时的c(CH3COOH)可近似视为仍等于0.010 mol/L)
(6)向明矾溶液中逐滴加入Ba(OH)2溶液至硫酸根离子刚好沉淀完全时,溶液的pH 7(填<、>、=), 离子反应总方程式为 。
向明矾溶液中逐滴加入Ba(OH)2溶液至铝离子刚好沉淀完全时,溶液的pH 7(填<、>、=), 离子反应总方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com