
【题目】下列有关说法正确的是( )
A. 苯酚钠溶液中通入少量的二氧化碳,产物是苯酚和碳酸钠
B. 苯的同系物中,苯环和侧链相互影响,使得二者均易被氧化
C. ![]() 在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2
在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2
D. 苯甲醛、苯乙烯分子中的所有原子可能处于同一平面
科目:高中化学 来源: 题型:
【题目】从2011年3月1日起,欧盟禁止生产含双酚A的塑料奶瓶。工业上双酚A系由苯酚和丙酮在酸性介质中制得: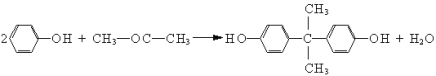 。下列说法中正确的是
。下列说法中正确的是
A. 该反应属于加成反应
B. 苯酚和双酚A都可以与NaHCO3反应
C. 苯酚有毒,但稀的苯酚溶液可用于杀菌消毒
D. 1mol苯酚和1mol双酚A最多都可以与3mol溴发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是 ( )
A. 铜铸塑像上出现铜绿[Cu2(OH)2CO3] B. 充有氢气的气球遇明火爆炸
C. 大理石雕像被酸雨腐蚀毁坏 D. 铁质菜刀生锈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中不正确的是( )
A.2.4g金属镁变成镁离子时失去的电子数为0.2NA
B.标准状况下,11.2 L CCl4所含分子数为0.5NA
C.常温常压下,28g N2中所含原子个数为2NA
D.16g O2和O3的混合气体中含氧原子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双极膜电渗析一步法盐制酸碱的技术进入到了工业化阶段,某科研小组研究采用BMED膜堆(如图所示),模拟以精制浓海水为原料直接制备酸和碱。BMED膜堆包括阳离子交换膜、阴离子交换膜和双极膜(a、d)已知:在直流电源的作用下,双极膜内中间界面层发生水的解离,生成H+和OH-。下列说法正确的是

A. 电极Y连接电源的正极,发生还原反应
B. I口排出的是混合碱,Ⅱ口排出的是淡水
C. 电解质溶液采用Na2SO4溶液可避免有害气体的产生
D. a左侧膜为阳离子交换膜,c为阴离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的不利影响。
(1)尿素[CO(NH2)2]是一种非常重要的高效氮肥,工业上以NH3、CO2为原料生产尿素,该反应实际为两步反应:
第一步:2NH3(g)+CO2(g) ![]() H2NCOONH4(s) △H=-272KJ·mol-1
H2NCOONH4(s) △H=-272KJ·mol-1
第二步:H2NCOONH4(s) ![]() CO(NH2)2(s)+H2O(g) △H=+138kJ·mol-1
CO(NH2)2(s)+H2O(g) △H=+138kJ·mol-1
写出工业上以NH3、CO2为原料合成尿素的热化学方程式:______________________。
(2)一定温度下,向2L恒容密闭容器中通入2molCO和1mol SO2,发生反应2CO(g)+SO2(g) ![]() 2CO2(g)+S(s)。若反应进行到20min时达平衡,测得CO2的体积分数为0.5,则前20min的反应速率v(CO)=_________,该温度下反应化学平衡常数K=__________。
2CO2(g)+S(s)。若反应进行到20min时达平衡,测得CO2的体积分数为0.5,则前20min的反应速率v(CO)=_________,该温度下反应化学平衡常数K=__________。

(3)工业上可用NaC1O碱性溶液或“亚硫酸盐法”吸收SO2。
①为了提高吸收效率,常用Ni2O3作为催化剂。催化过程如图所示:
a.过程2的离子方程式_______________________________。
b.Ca(C1O)2也可用于脱硫,且脱硫效果比NaC1O更好,原因是________________。
②室温条件下,将烟气通入(NH4)2SO4溶液中,测得溶液pH与含硫组分物质的量分数的变化关系如图所示,b点时溶液pH=7,则n(NH4+):n(SO32-)=__________。
(4)用食盐水做电解液电解烟气脱氮的原理如图,NO被阳极产生的氧化性物质氧化为NO3-,尾气经氢氧化钠溶液吸收后排入空气。如下图,电流密度和溶液pH对烟气脱硝的影响。

①NO被阳极产生的氧化性物质氧化为NO3-反应的离子方程式___________________。
②溶液的pH对NO去除率影响的原因是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烷烃的结构简式为![]() ,它的正确命名是( )
,它的正确命名是( )
A. 4-甲基-3-乙基戊烷 B. 3-丙基戊烷
C. 2-甲基-3-乙基戊烷 D. 3-乙基-2-甲基戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛在医药、染料、香料等行业中都有着广泛的应用。实验室通过下图所示的流程由甲苯氧化制备苯甲醛,试回答下列问题。

(1)Mn2O3氧化甲苯的反应需要不断搅拌,搅拌的作用是_______。
(2)甲苯经氧化后得到的混合物通过结晶、过滤进行分离,该过程中需将混合物冷却,其目的是_______。
(3)实验过程中,可循环使用的物质有_______、_______。
(4)实验中分离甲苯和苯甲醛采用的操作Ⅰ是______,其原理是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D四种分子所含原子的数目依次为1、3、6、2,且都含有18个电子,B、C是由两种元素的原子组成,且分子中两种原子的个数比均为1∶2。D物质的氢化物能刻蚀玻璃。
(1)A的分子式是________,写出A原子的价层电子排布式________。
(2)B分子的中心原子的杂化类型是________,分子空间构型是________,该分子属于________分子(填“极性”或“非极性”)。
(3)C的化学式是________,分子中含有的化学键类型是________。
(4)D物质的氢化物的沸点比HCl的沸点高,其主要原因是___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com