
| A. | 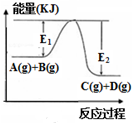 表示反应A(g)+B(g)→C(g)+D(g)是吸热反应,吸收能量(E2-E1)kJ | |
| B. | 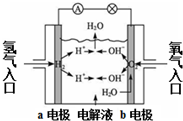 为氢氧燃料电池示意图,正、负极通入的气体体积之比为2:1 | |
| C. | 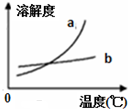 是物质a、b的溶解度曲线,可以用重结晶法从a、b混合物中提纯a | |
| D. | 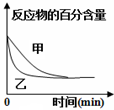 可表示压强对反应2A(g)+B(g)?3C(g)+D(s)的影响,且乙的压强大 |
分析 A.反应物的总能量大于生成物的总能量,属于放热发育;
B.正极反应物为氧气,负极为氢气,根据反应方程式判断;
C.溶解度随温度变化大的物质和变化小的物质可以采用重结晶的方法分离;
D.根据“先拐先平数值大”的方法确定压强大小,该反应是一个反应前后气体体积不变的反应,改变压强平衡不移动.
解答 解:A.该反应中,反应物的能量大于生成物能量,所以反应过程中要放出能量,即△H<0,故A错误;
B.氢氧燃料电池的反应方程式为:2H2+O2=2H2O,正极上通入氧气,负极上通入氢气,根据方程式知正、负极通入的气体体积之比为1:2,故B错误;
C.从图象可以看出,a物质的溶解度随着温度的降低而降低,并且降低非常明显,b的溶解度虽然也随温度的降低而降低,但是降低非常小,因此对于a物质和b物质的混合溶液来说,随着温度的降低,a就会大量的析出,所以可以采用重结晶的方法分离,故C正确;
D.根据图象知,乙条件下,先达到平衡,所以乙的压强度大于甲,由于D为固体,该反应是一个反应前后气体体积不变的反应,改变压强平衡不移动,所以反应物的百分含量不变,故D正确;
故选CD.
点评 本题考查图象分析题,题目涉及的知识点较多,侧重于考查学生对基础知识的综合应用能力,题目难度中等,易错选项是D,注意D选项中反应前后气体的计量数之和不变,为易错点.


科目:高中化学 来源: 题型:选择题
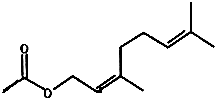
| A. | 分子式为C12H20O2 | |
| B. | 它的同分异构体中不可能有酚类 | |
| C. | 其一氯化物共7种 | |
| D. | 1mol该有机物与1mol水在一定条件下反应可能的产物有6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生铁中含有碳,抗腐蚀能力比纯铁强 | |
| B. | 钢铁发生析氢腐蚀时,负极反应是:Fe-3e-═Fe3+ | |
| C. | 在铁制品上镀铜时,镀件为阳极,铜盐为电镀液 | |
| D. | 铁管上镶嵌锌块,铁管不易被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XeF4分子具有非常好的热稳定性 | |
| B. | XeF4分子中Xe的化合价为0价 | |
| C. | 氧化剂和还原剂的物质的量之比为2:3 | |
| D. | 每生成4molXe转移16mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有AgCl和AgI固体的悬浊液:c(Ag+)>c(C1-)=c(I-) | |
| B. | CO2的水溶液:c(H+)>c(HCO3-)═2c(CO32-) | |
| C. | pH=1的NaHSO4溶液:c(H+)=c(SO42-)十c(OH-) | |
| D. | 含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)═2[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
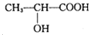 是人体生理活动的一种代谢产物.以下是采用化学方法对乳酸进行加工处理的过程,其中A、H、G为链状高分子化合物.请回答相关问题:
是人体生理活动的一种代谢产物.以下是采用化学方法对乳酸进行加工处理的过程,其中A、H、G为链状高分子化合物.请回答相关问题: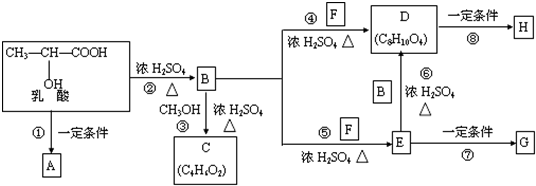
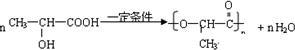
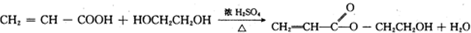
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
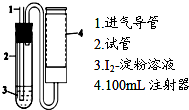 二氧化硫是造成大气污染的主要有害气体之一,某合作学习小组的同学拟测定某地大气中SO2的含量,实验步骤及装置如下:
二氧化硫是造成大气污染的主要有害气体之一,某合作学习小组的同学拟测定某地大气中SO2的含量,实验步骤及装置如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制氢气,为了加快反应速率,可向稀 H2SO4 中滴加少量 Cu(NO3)2 溶液 | |
| B. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变升高温度,平衡时氢气转化率增大 | |
| C. | 吸热反应“TiO2(s)+2Cl2(g)═TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反 应的△S<0 | |
| D. | 为处理锅炉水垢中的 CaSO4,可先用饱和 Na2CO3 溶液浸泡,再加盐酸溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素的单质一定是由还原该元素的化合物来制得 | |
| B. | 含有最高价元素的化合物不一定具有很强的氧化性 | |
| C. | 阳离子只能得到电子被还原,阴离子只能失去电子被氧化 | |
| D. | 在化学反应中,得电子越多的氧化剂,其氧化性就越强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com