
阅读下列内容,回答下题:
某药厂生产的胃药吗丁啉.其药效成分直接作用于胃肠壁而起效,可增加食道下部括约肌张力,防止胃,食道反流,增强胃蠕动,……它的结构简式可表示为如图所示
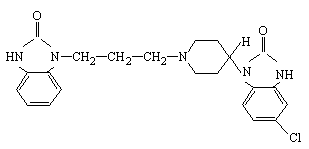
对于该物质,下列说法正确的是
[ ]
A.该物质具有碱性,能与酸反应
B.该物质不能发生加成反应
C.该物质不能发生取代反应
D.该物质属于盐类
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:阅读理解
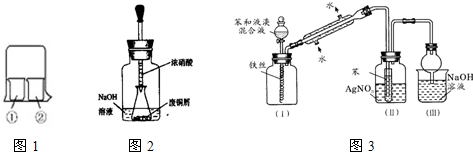
| 实验编号 | ①中的物质 | ②中的物质 |
| 1 | 淀粉碘化钾溶液 | 浓硝酸 |
| 2 | 酚酞溶液 | 浓硫酸 |
| 3 | 氯化铝溶液 | 浓氨水 |
| 4 | 湿润的红纸 | 饱和氯水 |
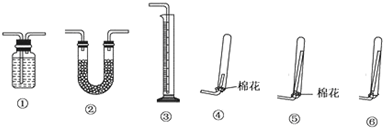
查看答案和解析>>
科目:高中化学 来源:2004全国各省市高考模拟试题汇编·化学 题型:013
阅读下列内容,回答下题:
某药厂生产的胃药吗丁啉.其药效成分直接作用于胃肠壁而起效,可增加食道下部括约肌张力,防止胃,食道反流,增强胃蠕动,……它的结构简式可表示为如图所示
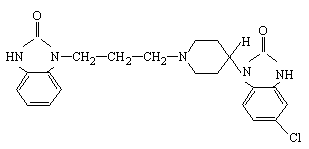
吗丁啉药效成分的分子式是
[ ]
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
有一包由硝酸钾和不溶性杂质组成的固体混合物,投入一定量的水中,在保证无水分蒸发的前提下,改变温度,测得固体混合物的溶解情况如下:
表一 实验结果
温度/℃ | 10 | 40 | 75 |
剩余固体质量/g | 261 | 175 | 82 |
表二 硝酸钾在不同温度时的溶解度
温度/℃ | 10 | 40 | 50 | 60 | 65 | 80 |
溶解度/g | 20.9 | 63.9 | 85.5 | 110 | 126 | 169 |
通过计算回答(要有计算过程):
(1)实验过程中所用水的质量是 。
(2)对75 ℃所得溶液的下列说法正确的是 。
A.该溶液是饱和溶液 B.该溶液是不饱和溶液
C.82 g剩余固体中含有硝酸钾 D.82 g剩余固体中不含硝酸钾
(3)原固体混合物中含硝酸钾的质量是 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年福建省漳州市芗城中学高二上学期期末考试化学试卷(带解析) 题型:实验题
阅读下列实验内容,根据题目要求回答问题:
某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100mL稀H2SO4溶液;以0.14 mol·L-1的NaOH溶液滴定上述稀H2SO4 25.00mL,滴定终止时消耗NaOH溶液15.00mL。
(1)该学生用标准0.14 mol·L-1NaOH溶液滴定硫酸的实验操作如下:
| A.用酸式滴定管取稀H2SO4 25.00mL,注入锥形瓶中,加入指示剂。 |
| B.用待测定的溶液润洗酸式滴定管。 |
| C.用蒸馏水洗干净滴定管。 |
| D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下。 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com