
 .
.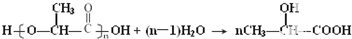 .
.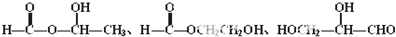 .
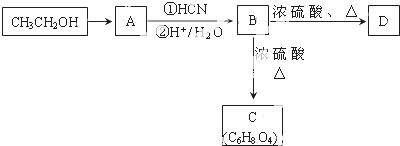
.分析 根据题中各物质的转化关系结合题中的信息可知,CH3CH2OH发生氧化反应得A为CH3CHO,A发生信息中的反应得B为CH3CHOHCOOH,B在浓硫酸作用下发生酯化反应得六元环C为 ,B发生缩聚反应得高分子D为
,B发生缩聚反应得高分子D为 ,据此答题.
,据此答题.
解答 解:根据题中各物质的转化关系结合题中的信息可知,CH3CH2OH发生氧化反应得A为CH3CHO,A发生信息中的反应得B为CH3CHOHCOOH,B在浓硫酸作用下发生酯化反应得六元环C为 ,B发生缩聚反应得高分子D为
,B发生缩聚反应得高分子D为 ,
,
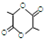
(1)根据上面的分析可知,B到C的反应类型是酯化反应,B到D的反应类型是缩聚反应,C的结构简式为 ,
,
故答案为:酯化反应;缩聚反应; ;
;
(2)由乙醇生成CH3CHO的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2H2O+2CH3CHO,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2H2O+2CH3CHO;
(3)D为 ,D在酸性条件下水解的化学方程式为
,D在酸性条件下水解的化学方程式为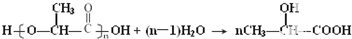 ,
,
故答案为: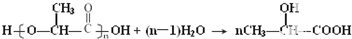 ;
;
(4)根据下列条件①能发生银镜反应,说明有醛基,②B能与金属钠反应,说明有羟基或羧基,③B中不含C-O-C键 ④一个碳原子上连有两个或三个羟基不稳定,说明一个碳上不能连两个或三个羟基,符合条件的所有同分异构体的结构简式为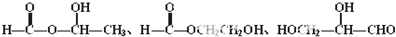 ,
,
故答案为: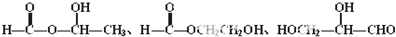 .
.
点评 本题考查有机推断与性质,题目难度中等,从合成条件和给出的信息分析可以得到各个点的结构,从而能够将各个题目破解,熟练掌握常见有机物结构与性质为解答关键.


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:选择题
| A. | 元素原子最外层电子排布呈周期性变化 | |
| B. | 元素相对原子质量依次递增 | |
| C. | 元素的最高正化合价呈周期性变化 | |
| D. | 元素原子半径大小呈周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

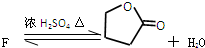
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)3CCH2OH | B. | CH3CH2C(CH3)2OH | C. | (CH3)3COH | D. | (CH3CH2)2CHOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
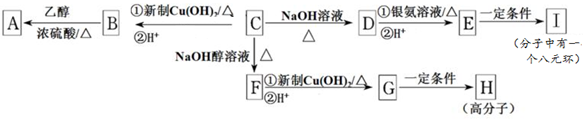
 ,I的结构简式是
,I的结构简式是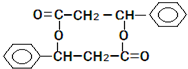 ,
, .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ②④ | C. | ①③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
| 半径(pm) | 30 | 64 | 66 | 70 | 106 | 108 | 128 | 186 | 232 |
| 主要化合价 | +1,-1 | -1 | -2 | -3,+5 | -2,+4,+6 | -3,+5 | +2 | +1 | +1 |
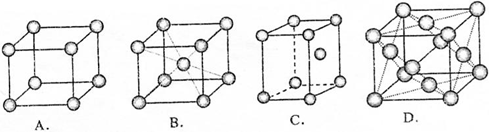
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com