
| A. | 浓硫酸 | B. | 浓磷酸 | ||
| C. | 浓硝酸 | D. | 浓的氢氧化钠溶液 |
科目:高中化学 来源: 题型:解答题
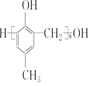 )的合成路线如图:
)的合成路线如图: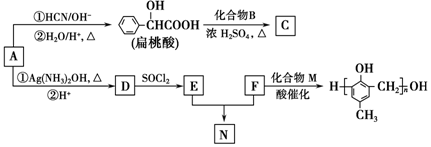
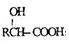
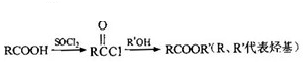
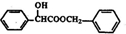 .
. )有多种同分异构体.属于甲酸酯且含酚羟基和亚甲基(-CH2-)的同分异构体共有3种,写出其中一种同分异构体的结构简式
)有多种同分异构体.属于甲酸酯且含酚羟基和亚甲基(-CH2-)的同分异构体共有3种,写出其中一种同分异构体的结构简式 (任意一种)..
(任意一种)..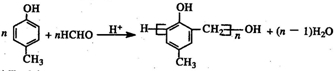
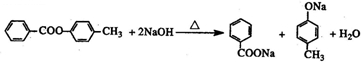 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氮及其化合物在工农业生产中具有重要作用.
氮及其化合物在工农业生产中具有重要作用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因浓硫酸具有强氧化性,故不可用它来干燥氢气 | |
| B. | 浓硫酸可用铁铝容器存放是因为常温下浓硫酸不与这两种金属反应 | |
| C. | 浓硫酸有强氧化性,稀硫酸不具有氧化性 | |
| D. | 实验室中利用浓硫酸的高沸点性来制备HCl等气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
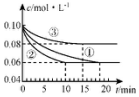
 如图装置实验,一段时间后某同学记录如下:
如图装置实验,一段时间后某同学记录如下:| A. | ③④⑤ | B. | ③④ | C. | ①②③ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸有强氧化性而稀硫酸无氧无性 | |
| B. | 98%的硫酸(密度1.84g/cm3)与18.4mol/L的硫酸的浓度不同 | |
| C. | 浓硫酸可以使胆矾晶体变白 | |
| D. | 浓硫酸与铜反应中,被氧化和被还原的物质的物质的量之比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应既是置换反应又是离子反应 | B. | 该反应转移了2e- | ||
| C. | Hg是氧化产物 | D. | HgS既是还原剂又是氧化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com