
以冶铝的废弃物铝灰为原料制取超细α-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下:
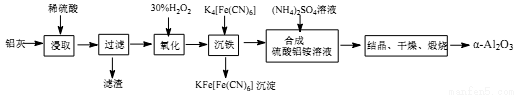
(1)铝灰中氧化铝与硫酸反应的化学方程式为_____________________;
(2)加30%的H2O2溶液的目的是_____________________;
(3)煅烧硫酸铝铵晶体,发生的主要反应为:
4[NH4Al(SO4)2•12H2O]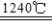 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过如下图所示的装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过如下图所示的装置。
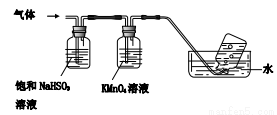
①集气瓶中收集到的气体是________(填化学式);
③KMnO4溶液褪色(MnO4-还原为Mn2+),此褪色过程中,氧化剂与还原剂的物质的量之比为________。
科目:高中化学 来源:2015-2016学年西藏日喀则一中高二月考化学试卷(解析版) 题型:选择题
2molFeCl2与1molCl2恰好完全反应,则转移的电子的物质的量为
A.4mol B.3mol C.2mol D.1mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高二下期末化学试卷(解析版) 题型:选择题
下列关于物质分类的说法正确的是
A.根据酸分子中含有的氢原子个数,将酸分为一元酸、二元酸和多元酸
B.混合物:铝热剂、福尔马林、水玻璃、漂白粉
C.根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素
D.明矾、水银、烧碱、硫酸均为强电解质
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二下期末化学试卷(解析版) 题型:选择题
下面的排序正确的是
A.晶体熔点:CF4>CCl4>CBr4>CI4
B.硬度:金刚石>晶体硅>碳化硅
C.沸点:HF<HCl<HBr<HI
D.晶格能由大到小:NaF>NaCl>NaBr>NaI
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二下期末化学试卷(解析版) 题型:选择题
下列说法中正确的是
A. 处于最低能量的原子叫做基态原子
B. 3s2表示3s能级有两个轨道
C. 同一原子中,1s、2s、3s电子的能量逐渐减小
D. 同一原子中,3d、4d、5d能级的轨道数依次增多
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南株洲二中等六校高二下期末化学试卷(解析版) 题型:选择题
下列说法正确的是
A.分子式为C9H10且含有碳碳双键的芳香烃有5种
B.结构为…-CH=CH-CH=CH-CH=CH-CH=CH-…的高分子化合物,其单体是乙烯
C.三分子甲醛合成三聚甲醛(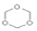 )的反应属于加成反应
)的反应属于加成反应
D.丙烯酸(CH2=CHCOOH)和山梨酸(CH3CH=CHCH=CHCOOH)不是同系物,它们与氢气充分后的产物也不是同系物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二下期末模拟化学试卷(解析版) 题型:选择题
已知反应CO(g)+2H2(g) CH3OH(g) △H=QkJ•mol-1,在三个不同容积的容器中分别充入1molCO与2molH2,恒温恒容,测得平衡时CO的转化率如下表。下列说法正确的是( )
CH3OH(g) △H=QkJ•mol-1,在三个不同容积的容器中分别充入1molCO与2molH2,恒温恒容,测得平衡时CO的转化率如下表。下列说法正确的是( )
温度(℃) | 容器体积 | CO转化率 | 平衡压强(P) | |
① | 200 | V1 | 50% | P1 |
② | 200 | V2 | 70% | P2 |
③ | 350 | V3 | 50% | P3 |
A.反应速率:③>①>②
B.平衡时体系压强:P1:P2=5:4
C.若容器体积V1>V3,则Q<O
D.若实验②中CO和H2用量均加倍,则CO转化率<75%
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西西北大学附中高二下期末化学试卷(解析版) 题型:填空题
A、B、C、D、E是周期表中前四周期的元素,其有关性质或结构信息如下表:
元素 | 有关性质或结构信息 |
A | 负二价的A元素的氢化物在通常状况下是一种液体,其中A的质量分数为88.9% |
B | B原子得到一个电子后3p轨道全充满 |
C | C原子的p轨道半充满,它的气态氢化物能与其最高价氧化物的水化物反应生成一种常见的盐X |
D | D元素的最高化合价与最低化合价的代数和为零,其最高价氧化物水化物的酸性为同主族最强 |
E | E元素的核电荷数等于A原子的核电荷数和B元素氢化物的核电荷数之和 |
(1)元素Y是C下一周期同主族元素,比较B、Y元素的第一电离能I1(B) I1(Y)(填“>”“=”或“<”);
(2)盐X的水溶液呈 (填“酸性”“碱性”或“中性”) ,原因________________(用离子方程式表示);
(3)E元素原子的核外电子排布式为_____________,在周期表中的位置______________;
(4)C单质分子中σ键和π键的个数比为 ,C的氢化物在同族元素的氢化物中沸点出现反常,其原因是____________________________________________;
(5)用高能射线照射液态H2A时,一个H2A分子能释放出一个电子,同时产生一种具有较强氧化性的阳离子,试写出该阳离子的电子式: ,写出该阳离子与硫的氢化物的水溶液反应的离子方程式:_________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com