
【题目】(1)如图是四种常见有机物的比例模型示意图。请按要求作答:
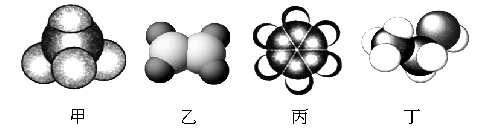
①甲的电子式为 ;乙的结构式为 ;
②戊是乙的一种同系物,相对分子质量为42,写出戊使溴水褪色的化学方程式
③丙分子中四个氢-子同时被溴-子取代得到种同分异构体
④丁是生活中常见有机物,请写出丁与食醋主要成分在浓硫酸催化并加热条件的化学反应方程式 。
(2)NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2。已知9.2gNO2和Na2CO3溶液完全反应时转移电子0.1mol,此反应的离子方程式是 。
【答案】(10分)
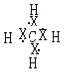
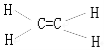
(1)①
②![]()
③3(2分)
④CH3COOH+HOCH2CH3![]() CH3COOCH2CH3+H2O(2分)
CH3COOCH2CH3+H2O(2分)
(2)2NO2+CO32-=NO3-+NO2-+CO2(2分)
【解析】
试题分析:(1)由四种常见有机物的比例模型示意图可知,甲为CH4,乙为CH2=CH2,丙为苯,丁为CH3CH3OH,
(1)①CH4的电子式为![]() ,乙烯的结构式为
,乙烯的结构式为![]() ,故答案为:
,故答案为:![]() ;
;![]() ;
;
②戊是乙的一种同系物,相对分子质量为42,由42/14=3可知,戊为CH3CH=CH2,与溴发生的加成反应为CH3CH=CH2+Br2→CH3CHBrCH2Br,故答案为:CH3CH=CH2+Br2→CH3CHBrCH2Br;
③苯中共6个H,4取代与2取代等效,苯上二元取代物有邻、间、对三种,则丙分子中四个氢原子同时被溴原子取代得到3种同分异构体,故答案为:3;
④丁与食醋主要成分在浓硫酸催化并加热条件的化学反应方程式为CH3COOH+HOCH2CH3![]() CH3COOCH2CH3+H2O。
CH3COOCH2CH3+H2O。
(2)9.2g NO2的物质的量为9.2/46=0.2mol,9.2gNO2和Na2CO3溶液完全反应时转移电子0.1mol,则每2molNO2和Na2CO3溶液反应时转移电子1mol,根据歧化反应的特点,N的化合价从+4价变化为+5价和+3价,即在碱性溶液中应生成NO3-和NO2-,所以反应的离子方程式为:2NO2+CO32-=NO3-+NO2-+CO2。


科目:高中化学 来源: 题型:
【题目】难溶电解质的溶解平衡属于化学平衡的一种。
(1)已知H2A在水中存在以下平衡:H2A![]() H++HA-,HA-
H++HA-,HA-![]() H++A2-。常温下CaA的饱和溶液中存在以下平衡:CaA(s)
H++A2-。常温下CaA的饱和溶液中存在以下平衡:CaA(s)![]() Ca2+(aq)+A2-(aq) ΔH>0,则该饱和溶液呈________性(填“酸”、“碱”或“中”),将溶液放入冰水浴中,则CaA的Ksp将_____(填“增大”、“减小”或“不变”,下同);滴加少量浓盐酸,c(Ca2+)________。
Ca2+(aq)+A2-(aq) ΔH>0,则该饱和溶液呈________性(填“酸”、“碱”或“中”),将溶液放入冰水浴中,则CaA的Ksp将_____(填“增大”、“减小”或“不变”,下同);滴加少量浓盐酸,c(Ca2+)________。
(2)含有Cr2O72-的废水毒性较大,某工厂废水中含5.00×10-3 mol·L-1的Cr2O72-。为使废水能达标排放,做如下处理:Cr2O72-Cr3+、Fe3+Cr(OH)3、Fe(OH)3。欲使10 L该废水中的Cr2O72-完全转化为Cr3+,则理论上需要加入________g FeSO4·7H2O。若处理后的废水中残留的c(Fe3+)=2×10-13 mol·L-1,则残留的Cr3+的浓度为________mol·L-1(已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.医用酒精的浓度通常为95%
B.单质硅是将太阳能转化为电能的常用材料
C.淀粉、纤维素和油脂都属于天然高分子化合物
D.合成纤维和光导纤维都是新型无机非金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为原电池装置示意图:

(1)若A为Zn,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式
(2)若A为铜片,B为石墨棒,电解质为FeCl3溶液,则铜片为 极(填正或负),写出正极电极反应式
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,该电池的总反应为 。当外电路有6.02X1022 个电子通过,则该电池正极消耗气体(标准状况) L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述Ⅰ和Ⅱ均正确并有因果关系的是
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | 1己醇的沸点比己烷的沸点高 | 1己醇和己烷可通过蒸馏初步分离 |
B | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
C | 乙二酸可与KMnO4溶液发生反应 | 乙二酸具有酸性 |
D | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期A、B、C、D、E5种主族元素,-子序数依次增大,A是元素周期表中原子半径最小元素,B元素最高价氧化物分子式为B2O5;C的阴离子和D的阳离子具有相同的电子层结构,E的L层电子数等于K、M两个电子层上电子数之和。
(1)元素:A为 ,B为
(2)E在周期表中的位置为
(3)C、D两元素的单质反应,生成一种淡黄色的固体F,则F的化学式为是 ,属于 化合物(填“离子”或“共价”),该化合物中阴阳离子数比为
(4)单质C怎能溶于元素B最高价氧化物对应水化物的稀溶液,请写出该反应离子方程式
(5)E 的一种氧化物为酸雨的“罪魁祸首”。设计一实验证明某气体为E 的该氧化物,并写出该氧化物与足量NaOH的反应离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是( )
A.CaCO3溶于醋酸溶液:CaCO3+2H+===Ca2++H2O+CO2↑
B.钠与CuSO4溶液反应:2Na + Cu2+ = Cu + 2Na+
C.已知:酸的强弱H2CO3>HClO>HCO![]() ,则:2ClO-+ CO2(少量) + H2O ===CO32-+ 2HClO
,则:2ClO-+ CO2(少量) + H2O ===CO32-+ 2HClO
D.将足量的NaHCO3溶液加入少量澄清石灰水中:Ca2+ + 2OH- + 2HCO![]() = CaCO3↓ + 2H2O+ CO32-
= CaCO3↓ + 2H2O+ CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一无色透明溶液,可能含Al3+、Fe3+、Cu2+、Mg2+、K+、OH-、CO32-、Cl-离子中的若干种。现做如下实验:
(1)取少量该溶液,滴入用硝酸酸化的AgNO3溶液,有白色沉淀生成。
(2)另取部分溶液,加入氢氧化钠,有白色沉淀产生,加入氢氧化钠的量与生成白色沉淀的量可用下图表示。

试推断:
①该溶液中以上离子一定存在的有__________,一定不存在的有__________。
②上述溶液中至少由___________、__________(填化学式)等溶质混合而成,其物质的量比为__________。
③写出图中a→b变化过程的离子方程式_____________________。
④为进一步确定溶液中其他的阳离子,应该补充的实验操作和结论是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”,凡有一个手性碳原子的物质一定具有光学活性,物质 经过以下反应仍具有光学活性的是
经过以下反应仍具有光学活性的是
A.与乙酸发生酯化反应 B.与NaOH水溶液反应
C.与银氨溶液作用只发生银镜反应 D.在催化剂作用下与H2加成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com