
 是一种取代有机氯农药DDT杀虫剂,其分子式为C15H22O3,它含有3种官能团,官能团的名称分别是碳碳双键、羟基、醛基
是一种取代有机氯农药DDT杀虫剂,其分子式为C15H22O3,它含有3种官能团,官能团的名称分别是碳碳双键、羟基、醛基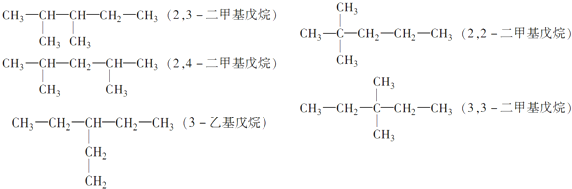 .
. 分析 (1)依据该化合物的结构简式确定分子式,此有机物中含有的官能团有C=C、-CHO、-OH;
(2)根据相对分子质量为100,确定C原子个数,根据主链上有5个碳原子的碳链异构体的书写方法来确定同分异构体的数目以及命名.
解答 解:(1)该化合物中含有15个C、22个H和3个O,故分子式为:C15H22O3,此有机物中含有的官能团有C=C、-CHO、-OH,所以其官能团种类是3,名称分别为碳碳双键、醛基和羟基,故答案为:C15H22O3;3;碳碳双键、羟基、醛基;
(2)相对分子质量为100的烃,100÷14=7余2,故符合烷烃的通式:CnH2n+2,即14n+2=100,解得n=7,即为庚烷,主链上有5个碳原子的同分异构体有:2,3-二甲基戊烷,2,4-二甲基戊烷,2,2-二甲基戊烷,3,3-二甲基戊烷,3-乙基戊烷,共5种,故答案为:
点评 本题考查了有机物的结构,知道常见有机物官能团类型即可解答,中学教材中常见的有机物官能团有:C=C、醛基、羟基、酯基、羧基、氨基、肽键、羰基等,题目难度不大.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案科目:高中化学 来源: 题型:填空题
 元素在周期表中的位置,反映了元素的原子结构和元素的性质,下图是元素周期表的一部分:
元素在周期表中的位置,反映了元素的原子结构和元素的性质,下图是元素周期表的一部分: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题


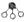 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面、在催化剂表面N2、H2中的化学键断裂.
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面、在催化剂表面N2、H2中的化学键断裂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCOOC2H5 CH3CH2COOH | B. | 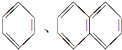 | ||
| C. | O2、O3 | D. | H、D、T |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1s22s22p4 | B. | 1s22s22p63s23p3 | ||
| C. | 1s22s22p3 | D. | 1s22s22p63s23p64s2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原固体混合物中NaHCO3的物质的量为0.2mol | |
| B. | 固体残渣的成分为NaOH和Na2CO3的混合物 | |
| C. | 原固体混合物中NaOH和NaHCO3的物质的量之比为2﹕5 | |
| D. | 原固体混合物中加入过量盐酸会放出5.6L气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com