
| A. | 设法将太阳光聚焦,产生高温,使水分解产生氢气 | |
| B. | 寻找特殊化学物质,使水分解产生氢气,同时释放能量 | |
| C. | 寻找特殊化学物质,用于开发廉价能源以分解水制取氢气 | |
| D. | 构成水的氢气和氧气都是可燃烧的物质,因此可研究在水不分解的情况下,使氢能成为二级能源 |
分析 A.高温条件下水分解产生氢气和氧气;
B.特殊化学物质如催化剂能加快化学反应速率,但水的分解是吸热反应;
C.开发廉价能源,以分解水制氢气可以降低成本;
D.水不分解就不能得到氢气,也就得不到二次能源.
解答 解:A.高温下水分解产生氢气,设法将太阳光聚焦,产生高温,使水分解产生氢气是可行的,故A正确;
B.特殊化学物质如催化剂能加快化学反应速率,水分解产生氢气,但水的分解是吸热反应,故B错误;
C.寻找特殊化学物质,开发廉价能源以分解水制氢气,可以降低成本,这是可行的,故C正确;
D.水不分解就不能得到氢气,也就不能使氢能成为二级能源,故D错误;
故选BD.
点评 本题考查了能源的分类、化学反应中的能量变化、水的组成等,题目难度不大,注意水分解时要吸收能量.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ⑤>②>④>③>① | B. | ④>①>③>②>⑤ | C. | ⑤>④>②>①>③ | D. | ④>③>⑤>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②⑤ | C. | ③⑤⑥ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | |||||||
| ① | |||||||
| Li | C | ④ | ⑤ | ⑥ | |||
| ⑦ | ⑧ | ⑨ | ⑩ | ||||
| K | ⑫ | ⑬ | |||||
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
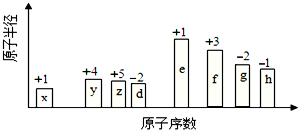 随原子序数的递增的八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如图所示.
随原子序数的递增的八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如图所示. .
.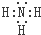 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 仅由实验②即可推断原混合溶液中一定存在Fe3+ | |
| B. | 要确定原混合溶液是否含有ClO- 至少需完成实验①②③ | |
| C. | 该溶液阳离子中一定存在Na+、Fe2+、Fe3+,一定不存在Al3+,无法确定是否含有K+ | |
| D. | 溶液中阴离子只有SO42-,且c(SO42-)大于2.75moL/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com