
A.1∶1 B.1∶
科目:高中化学 来源: 题型:
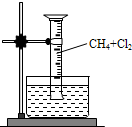 某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.
某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.查看答案和解析>>
科目:高中化学 来源:2013届福建省三明一中、二中高三上学期期末联考化学试卷(带解析) 题型:填空题
合成氨尿素工业生产过程中涉及到的物质转化过程如下图所示。
(1)天然气(主要成分为CH4)在高温、催化剂作用下与水蒸气反应生成H2和CO的化学方程式为 。
(2)甲烷是一种清洁燃料,但不完全燃烧时热效率降低,同时产生有毒气体造成污染。
已知:CH4(g) + 2O2(g)=CO2(g) + 2H2O(l) ΔH1=―890.3 kJ/mol
2CO (g) + O2(g)=2CO2(g) ΔH2=―566.0 kJ/mol
则甲烷不完全燃烧生成一氧化碳和液态水时的热效率是完全燃烧时的_____倍(计算结果保留1位小数)。
(3)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50 mL 2 mol·L-1的氯化铜溶液的装置示意图: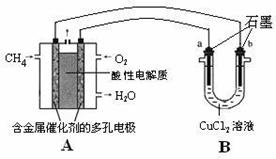
请回答:
①甲烷燃料电池的正极反应式是____ ____。
②当线路中有0.1 mol电子通过时,________(填“a”或“b”)极增重________g。
(4)运输氨时,不能使用铜及其合金制造的管道阀门。因为在潮湿的环境中,金属铜在有NH3存在时能被空气中的O2氧化,生成[Cu(NH3)4]2+,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2009-2010学年河北冀州中学高一下学期期中考试化学卷 题型:填空题
填空题
(1)下列说法中正确的是
①门捷列夫绘制出了第一张我们现在常用的元素周期表。②天然存在的同位素,相互间保持一定的比率。③元素的性质随着原子量的递增而呈周期性变化的规律叫做元素周期律。④燃料电池与干电池的主要差别在于反应物不同。⑤同系物之间分子量相差14。⑥由于存在化学反应的限度,所以一个化学反应在实际进行时不一定按照化学方程式的计量关系进行。⑦各种物质都储存有化学能。⑧甲烷和氯水在光照条件下发生取代反应,产物为混合物。
(2)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片
的质量减少了3.25克,铜表面析出了氢气 L(标准状况下),导线中通过 mol电子。
(3)在25℃时,向100 mL含氯化氢14.6 g的盐酸溶液里放入5.60 g纯铁粉(不考虑反应前后溶液体积的变化),反应开始至2 min末,收集到1.12 L(标准状况)氢气。在此之后,又经过4 min,铁粉完全溶解。则: 前2 min与后4 min相比,反应速率较快的是 ,其原因是
(4)已知下列原电池的总反应式:Cu+2FeCl3==CuCl2+2FeCl2,请写出电极反应方程式:
正极反应方程式为:
负极反应方程式为:
(5)已知断开1 molH-H键、1mol Br-Br键、1mol H-Br键分别需要吸收的能量为436kJ、193kJ、366kJ.。 计算H2和Br2反应生成1mol HBr需_______(填“吸收”或“放出”)能量_______kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
填空题
(1)下列说法中正确的是
①门捷列夫绘制出了第一张我们现在常用的元素周期表。②天然存在的同位素,相互间保持一定的比率。③元素的性质随着原子量的递增而呈周期性变化的规律叫做元素周期律。④燃料电池与干电池的主要差别在于反应物不同。⑤同系物之间分子量相差14。⑥由于存在化学反应的限度,所以一个化学反应在实际进行时不一定按照化学方程式的计量关系进行。⑦各种物质都储存有化学能。⑧甲烷和氯水在光照条件下发生取代反应,产物为混合物。
(2)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片
的质量减少了3.25克,铜表面析出了氢气 L(标准状况下),导线中通过 mol电子。
(3)在25℃时,向100 mL含氯化氢14.6 g的盐酸溶液里放入5.60 g纯铁粉(不考虑反应前后溶液体积的变化),反应开始至2 min末,收集到1.12 L(标准状况)氢气。在此之后,又经过4 min,铁粉完全溶解。则: 前2 min与后4 min相比,反应速率较快的是 ,其原因是
(4)已知下列原电池的总反应式:Cu+2FeCl3==CuCl2+2FeCl2,请写出电极反应方程式:
正极反应方程式为:
负极反应方程式为:
(5)已知断开1 molH-H键、1mol Br-Br键、1mol H-Br键分别需要吸收的能量为436kJ、193kJ、366kJ.。 计算H2和Br2反应生成1mol HBr需_______(填“吸收”或“放出”)能量_______kJ。
查看答案和解析>>
科目:高中化学 来源:2009—2010学年河北冀州中学高一下学期期中考试化学卷 题型:填空题
填空题
(1)下列说法中正确的是
①门捷列夫绘制出了第一张我们现在常用的元素周期表。②天然存在的同位素,相互间保持一定的比率。③元素的性质随着原子量的递增而呈周期性变化的规律叫做元素周期律。④燃料电池与干电池的主要差别在于反应物不同。⑤同系物之间分子量相差14。⑥由于存在化学反应的限度,所以一个化学反应在实际进行时不一定按照化学方程式的计量关系进行。⑦各种物质都储存有化学能。⑧甲烷和氯水在光照条件下发生取代反应,产物为混合物。
(2)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片
的质量减少了3.25克,铜表面析出了氢气 L(标准状况下),导线中通过 mol电子。
(3)在25℃时,向100 mL含氯化氢14.6 g的盐酸溶液里放入5.60 g纯铁粉(不考虑反应前后溶液体积的变化),反应开始至2 min末,收集到1.12 L(标准状况)氢气。在此之后,又经过4 min,铁粉完全溶解。则:前2 min与后4 min相比,反应速率较快的是 ,其原因是
(4)已知下列原电池的总反应式:Cu+2FeCl3==CuCl2+2FeCl2,请写出电极反应方程式:
正极反应方程式为:
负极反应方程式为:
(5)已知断开1 mo lH-H键、1mol Br-Br键、1mol H-Br键分别需要吸收的能量为436kJ、193kJ、366kJ.。 计算H2和Br2反应生成1mol HBr需_______(填“吸收”或“放出”)能量_______kJ。
lH-H键、1mol Br-Br键、1mol H-Br键分别需要吸收的能量为436kJ、193kJ、366kJ.。 计算H2和Br2反应生成1mol HBr需_______(填“吸收”或“放出”)能量_______kJ。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com