
【题目】将8.0 g铁粉加入到100 mL 2.0 mol/L FeCl3溶液中,发生反应为Fe+2Fe3+=3Fe2+,反应后过滤、洗涤、烘干得固体质量为m。下列说法不正确的是( )
A.m=2.4gB.Fe3+在反应中做氧化剂,失去0.2mol电子
C.该反应是化合反应D.反应后溶液中n(Fe2+)=0.3 mol
科目:高中化学 来源: 题型:
【题目】氮及其化合物的转化过程如图所示,下列分析合理的是

A. 催化剂a表面发生了极性共价键的断裂和形成
B. 在催化剂b表面形成氮氧键时,不涉及电子转移
C. N2与H2反应生成NH3的原子利用率为100%
D. 催化剂a、b能提高反应的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着石油资源的日趋紧张,天然气资源的开发利用受到越来越多的关注。以天然气(主要成分是CH4)为原料经合成气(主要成分为CO、H2)制化学品,是目前天然气转化利用的主要技术路线。而采用渣油、煤、焦炭为原料制合成气,常因含羰基铁[Fe(CO)5]等而导致以合成气为原料合成甲醇和合成氨等生产过程中的催化剂产生中毒。请回答下列问题:
(1)[Fe(CO)5]中铁的化合价为0,写出铁原子的基态电子排布式:_____________________。
(2)与CO互为等电子体的分子和离子分别为________和________(各举一种即可,填化学式),CO分子的电子式为________,CO分子的结构式可表示成________。
(3)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有___,CH3OH的熔、沸点比CH4高,其主要原因是__________。
(4)CH3CHO分子中,—CH3中的碳原子采取________杂化方式,—CHO中的碳原子采取________杂化方式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个密闭容器中,中间有一可自由滑动的隔板,将容器分成两部分。当左边充入28克N2,右边充入8克CO和CO2的混合气体时,隔板处于如图所示位置(两侧温度相同)。下列说法正确的是

A.右边CO和CO2的分子数之比为1∶3
B.右边CO的质量为2.75克
C.若改变右边CO和CO2的充入量而使隔板处于距离右端1/6处,保持温度不变,则前后两次充入密闭容器内的气体总压强之比为25∶24
D.右侧气体密度是相同条件下氢气密度的32倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 若把H2S分子写成H3S分子,违背了共价键的饱和性
B. H3O+离子中存在配位键
C. 已知X、Y元素同周期,且电负性X>Y, 第一电离能X一定大于Y
D. 在面心立方堆积的金属晶体中,属于1个晶胞的金属原子有4个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式中,不能正确表达反应颜色变化的是( )
A.向CuSO4溶液中加入足量Zn粉,溶液蓝色消失:Zn+CuSO4=Cu+ZnSO4
B.澄清的石灰水久置后出现白色固体:Ca(OH)2+CO2=CaCO3↓+H2O
C.将饱和氯化铁溶液滴入沸水中得到红褐色分散系:FeCl3+3H2O![]() Fe(OH)3↓+3HCl
Fe(OH)3↓+3HCl
D.向CuO粉末中加入碳粉加热得到红色固体:2CuO+C![]() 2Cu+CO2↑
2Cu+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察图示,然后回答问题:
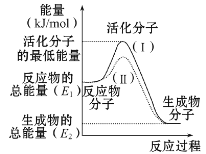
①图中所示反应是________(填“吸热”或“放热”)反应,该反应________ (填“需要”或“不需要”)加热,该反应的ΔH=________ (用含E1、E2的代数式表示)。
②已知热化学方程式:H2(g)+ ![]() O2(g)====H2O(g) ΔH=-241.8 kJ/mol。该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为_____________。
O2(g)====H2O(g) ΔH=-241.8 kJ/mol。该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为_____________。
(2)有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A.CH3OH(g)+H2O(g)====CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
B.CH3OH(g)+ ![]() O2(g)====CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol
O2(g)====CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol
另外H2O(l)====H2O(g) ΔH=+44 kJ/mol,请写出32 g 的CH3OH(g)完全燃烧生成液态水的热化学方程式______________________。
(3)已知反应2HI(g)![]() H2(g)+I2(g)的ΔH=+11 kJ·mol-1,1 mol H2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(g)分子中化学键断裂时需吸收的能量为__kJ。
H2(g)+I2(g)的ΔH=+11 kJ·mol-1,1 mol H2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(g)分子中化学键断裂时需吸收的能量为__kJ。
(4)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) ΔH1
CH3OH(g) ΔH1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH3
CO(g)+H2O(g) ΔH3
已知反应①中相关的化学键键能数据如下:
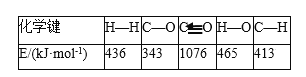
由此计算ΔH1=____kJ·mol-1;已知ΔH2=-58 kJ·mol-1,则ΔH3=____kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.22.4L气体所含的分子数一定大于11.2L气体所含的分子数
B.常温常压下, 由O3与O2组成的混合气体48g含有的原子数为3NA
C.标准状况下,33.6L 四氯化碳(CCl4)中含有的碳原子数目为1.5NA
D.常温常压下,7.1 g Cl2与足量的Fe充分反应,转移的电子数目为0.3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一个绝热恒容密闭容器中通入CO(g)和H2O(g),一定条件下使反应CO(g)+H2O(g)![]() CO2(g)+H2(g)达到平衡,正反应速率随时间变化的曲线如图所示,由图可得出的结论正确的是
CO2(g)+H2(g)达到平衡,正反应速率随时间变化的曲线如图所示,由图可得出的结论正确的是

A. 反应物浓度:a点小于c点
B. 该反应的正反应为放热反应
C. c点达到平衡状态
D. Δt1=Δt2时,H2的产率:a~b段大于b~c段
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com