
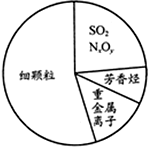
| A、苯是最简单的芳香烃 |
| B、重金属离子可导致蛋白质变性 |
| C、SO2和NxOy均属于酸性氧化物 |
| D、大量燃烧化石燃料是造成雾霾天气的一种重要因素 |


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2:3 | B、3:1 |
| C、1:2 | D、1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、高纯度的硅广泛用于制作计算机 |
| B、硅可由二氧化硅还原制得 |
| C、低温时,硅与水、空气和酸不反应,但能与氢氟酸反应 |
| D、自然界中硅的储量丰富,自然界中存在大量的单质硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;
(1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
| c(CO) |
| c(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、负极的反应式为CH3OH+H2O-6e-═CO2↑+6H+ |
| B、电池的反应方程式是2CH3OH+3O2═2CO2+4H2O |
| C、电池工作时,H+由正极移向负极 |
| D、电池工作时,电子从通入甲醇的一极流出,经外电路再从通入氧气的一极流入 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、第8min时 A的反应速率为0.08mol?L-1?min-1 |
| B、在0-54分钟的反应过程中该可逆反应的平衡常数始终为4 |
| C、30min时改变的条件是降低温度,40min时改变的条件是升高温度 |
| D、反应方程式中的x=1,且正反应为放热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com