(2009?广州二模)二氧化钛(TiO
2)广泛用于制造高级白色油漆,也是许多反应的催化剂.工业上用钛铁矿[主要成分为FeTiO
3(钛酸亚铁,不溶于水)、Fe
2O
3及少量SiO
2杂质]作原料,制取二氧化钛及绿矾,其生产流程如下:
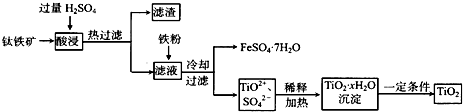
回答下列问题:
(1)Ti原子核外电子层数为4,位于元素周期表第ⅣB族.Ti原子序数为
22
22
.
(2)FeTiO
3溶于过量硫酸的离子方程式
FeTiO3+4H+=Fe2++TiO2++2H2O
FeTiO3+4H+=Fe2++TiO2++2H2O
.
(3)流程中生成TiO
2?xH2O离子方程式为
TiO2++(x+1)H2O=TiO2?xH2O+2H+
TiO2++(x+1)H2O=TiO2?xH2O+2H+
.
(4)若铁粉的用量不足,可能导致产品TiO
2中混有
Fe2O3
Fe2O3
杂质.
(5)以TiO
2为原料制取金属钛的其中一步反应为TiO
2+Cl
2+C
TiCl
4+
2CO
2CO
,已知该反应中氧化剂与还原剂的物质的量之比为1:1,则另一生成物为
CO
CO
.



