
 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的KI溶液、足量的CuSO4溶液和K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得乙中c电极质量增加32g.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的KI溶液、足量的CuSO4溶液和K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得乙中c电极质量增加32g.据此回答问题:分析 (1)该装置是电解池,接通电源,经过一段时间后,乙中c电极质量增加32g,说明c电极是电解池阴极,则d电极是阳极,连接电解池阳极的原电池电极是正极;
(2)电解KI溶液时,阳极上碘离子失电子发生氧化反应生成碘单质;
(3)电解K2SO4溶液时,电极f为阳极即氢氧根离子放电生成氧气,根据得失电子守恒计算;
(4)甲烧杯为电解KI溶液,阳极碘离子失电子发生氧化反应生成碘单质,碘单质遇淀粉溶液变蓝;
(5)甲溶液为电解KI溶液生成碘单质、氢氧化钾和氢气,乙溶液为电解CuSO4溶液生成铜单质、硫酸和氧气.
解答 解:(1)该装置是电解池,接通电源,经过一段时间后,乙中c电极质量增加32g,说明c电极是电解池阴极,则电源的N端为正极,故答案为:正;
(2)电解KI溶液时,阳极上碘离子失电子发生氧化反应生成碘单质,电极反应式为:2I--2e-=I2,故答案为:2I--2e-=I2;
(3)电解K2SO4溶液时,电极f为阳极即氢氧根离子放电生成氧气,电极反应式为:4OH--4e-=2H2O+O2↑,又c电极质量增加32g即析出32g铜,所以根据得失电子守恒,电极f上生成的气体在标准状况下的体积为$\frac{32}{64}$×$\frac{1}{2}$×22.4=5.6L,故答案为:5.6L;
(4)甲烧杯为电解KI溶液,阳极碘离子失电子发生氧化反应生成碘单质,所以在甲烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是溶液变蓝,故答案为:溶液变蓝;
(5)甲溶液为电解KI溶液生成碘单质、氢氧化钾和氢气,乙溶液为电解CuSO4溶液生成铜单质、硫酸和氧气,所以电解前后甲溶液的pH增大,乙溶液的pH减小,故答案为:增大; 减小.
点评 本题为电化学知识的综合应用,做题时要注意根据电极反应现象判断出电解池的阴阳级,进而判断出电源的正负极,要注意三个电解池为串联电路,各电极上得失电子的数目相等,做题时要正确写出电极方程式,准确判断两极上离子的放电顺序.


科目:高中化学 来源: 题型:填空题
 表示的分子式为C6H14,名称是2-甲基戊烷,从碳骨架来看,属于烷烃.它的含四个甲基的同分异构体的结构简式为
表示的分子式为C6H14,名称是2-甲基戊烷,从碳骨架来看,属于烷烃.它的含四个甲基的同分异构体的结构简式为 、
、 .
. 中含有的官能团的名称为羟基、酯基,分子式为C8H8O2.
中含有的官能团的名称为羟基、酯基,分子式为C8H8O2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4和NH4+是等电子体,键角均为109°28′ | |
| B. | NO3-和CO32-是等电子体,均为平面正三角形结构 | |
| C. | H3O+和PCl3是等电子体,均为三角锥形结构 | |
| D. | B3N3H6和苯是等电子体,B3N3H6分子中存在“肩并肩”式重叠的轨道 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ③ | C. | ②③ | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
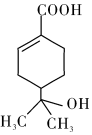 某有机物的结构简式如图所示,下列有关该有机物的说法不正确的是( )
某有机物的结构简式如图所示,下列有关该有机物的说法不正确的是( )| A. | ①②③④⑤ | B. | ①②⑤⑥ | C. | ①②④⑤⑥ | D. | 全部不正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com