
| A、Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
| B、腐蚀法制作印刷线路板2Fe3++Cu═2Fe2++Cu2+ |
| C、碳酸氢铵溶液中加足量石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| D、用惰性电极电解熔融氯化钠:2Cl-+2H2O═Cl2↑+H2↑+2OH- |
| ||


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
| A、误食重金属盐引起人体中毒,可喝大量的食盐水解毒 |
| B、变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应 |
| C、浸泡过高锰酸钾溶液的硅藻土放于水果箱内是为了延长水果保鲜期 |
| D、安装煤炭燃烧过程的“固硫”装置,主要是为了提高煤的利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol乙烯和乙醇的混合物完全燃烧所消耗的O2一定为0.3NA |
| B、常温常压下,46g NO2与N2O4的混合气体中含有的分子总数为NA |
| C、25℃时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.1NA |
| D、一定量的钠与8g氧气作用,若两者均无剩余,转移NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、通过浓硫酸除去HCl中的H2O |
| B、通过灼热的CuO除去H2中的CO |
| C、通过灼热的镁粉除去N2中的O2 |
| D、通过水除去CO中的CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol N2与足量的H2反应,转移的电子数是0.6NA |
| B、常温下,0.1mol?L-1 NH4NO3溶液中含有的氮原子数是0.2NA |
| C、常温常压下,3.2g O2和3.2g O3所含氧原子数都是0.2NA |
| D、2.24L CO和CO2的混合气体中所含的碳原子数为0.1N A |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
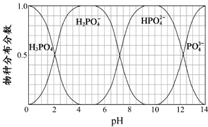 磷和砷是同主族的非金属元素.
磷和砷是同主族的非金属元素.查看答案和解析>>
科目:高中化学 来源: 题型:
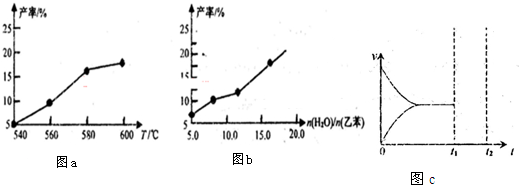
| n(H2O) |
| n(乙苯) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、工业上,用焦炭在高温下还原二氧化硅制得粗硅 |
| B、“玉兔号”月球车太阳能电池帆板的材料是二氧化硅 |
| C、地沟油的主要成分是油脂,其组成与汽油、煤油不相同 |
| D、钠可把钛、锆、铌、钽等金属从它们的熔融的卤化物里还原出来 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com