
 早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为:4NaOH(熔融)═4Na+O2↑+2H2O;后来盖?吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH═Fe3O4+2H2↑+4Na↑.下列有关说法正确的是( )
早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为:4NaOH(熔融)═4Na+O2↑+2H2O;后来盖?吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH═Fe3O4+2H2↑+4Na↑.下列有关说法正确的是( )| A、电解熔融氢氧化钠制钠,阳极发生电极反应为:4OH--4e-=O2↑+2H2O |
| B、盖?吕萨克法制钠原理是利用铁的还原性比钠强 |
| C、若戴维法与盖?吕萨克法制得等量的钠,则两反应中转移的电子总数也相同 |
| D、目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阴极,铁为阳极 |
| ||
| ||
| ||
| ||


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源: 题型:
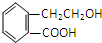 ,它可通过不同化学反应分别制得B、C、D和E四种物质.
,它可通过不同化学反应分别制得B、C、D和E四种物质.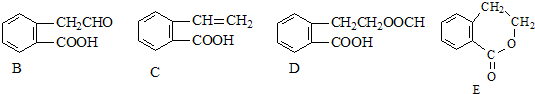
查看答案和解析>>
科目:高中化学 来源: 题型:
A、NaCl的电子式: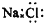 |
| B、乙烯的结构式:CH2=CH2 |
C、S2-结构示意图: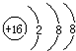 |
D、CH4分子的球棍模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:
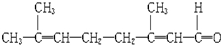 ,判断下列有关说法中不正确的是( )
,判断下列有关说法中不正确的是( )| A、它可以使酸性高锰酸钾溶液褪色 |
| B、它可以使溴水褪色 |
| C、它与银氨溶液发生反应生成银镜 |
| D、它的催化加氢反应产物的分子式为C10H20O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在金属和非金属的分界线附近可以找到半导体材料 |
| B、第ⅣA族所有含氧酸的钠盐,溶于水均呈碱性 |
| C、如果已知元素的最外层电子数为2,由此不能判断该元素在周期表中的位置 |
| D、目前已知发现的第ⅣA族元素为5种,所以该族元素共有5种单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
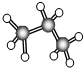 如图是某烷分子的球棍模型图,图中大、小“球”表示两种元素的原子,“棍”表示化学键.其结构简式是( )
如图是某烷分子的球棍模型图,图中大、小“球”表示两种元素的原子,“棍”表示化学键.其结构简式是( )| A、CH3CH3 |
| B、CH3CH2CH3 |
| C、CH3CH2CH2CH3 |
| D、CH2CH3CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 起始浓度/(mol?L-1) | 反应后溶液的pH | 结论 | |
| c(HA) | c(KOH) | |||
| A. | 0.1 | 0.1 | 7 | HA为弱酸 |
| B. | 0.1 | 0.1 | 9 | c(K+)<c(A-) |
| C. | 0.2 | 0.1 | 6 | HA为强酸 |
| D. | 0.2 | 0.1 | 8 | C(A-)<c(HA) |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
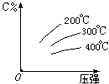 可逆反应mA (g)+nB(s)?eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )
可逆反应mA (g)+nB(s)?eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )| A、达平衡后,加入催化剂,加快反应速率,使C%增大 |
| B、达平衡后,增加B的量有利于平衡向正反应方向移动 |
| C、化学方程式中m+n<e+f |
| D、该可逆反应的正反应的△H<0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com