
【题目】下图为实验室制乙烯(A)、硝基苯(B)和石油分馏(C)的装置:
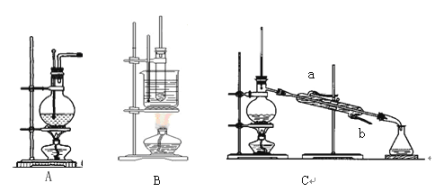
(1)写出制取乙烯、硝基苯的化学方程式:___________、_________。
(2)在A和 C实验中需加碎瓷片,其目的是_______________。
(3)分离试验B中硝基苯的方法是__________。
(4)在石油分馏实验中,冷凝水的流向应是_______进______出(填字母a、b)。
(5)实验室制乙烯时,常伴随有刺激性气味的气体产生,为消除其对乙烯性质实验的干扰,可将气体通过_______溶液除去。若反应没有及时升温至170℃,可能带来的主要副产物是____(填名称)。
【答案】CH3CH2OH![]() CH2=CH2↑+H2O
CH2=CH2↑+H2O ![]() 防止暴沸 分液 b a 氢氧化钠, 乙醚
防止暴沸 分液 b a 氢氧化钠, 乙醚
【解析】
(1)制取乙烯、硝基苯的化学方程式分别为:![]()
![]() ;
;
(2)给液体加热的实验,要防止暴沸。在A和 C实验中需加碎瓷片,其目的是:防止暴沸;
(3)硝基苯与浓硝酸、浓硫酸等不相溶,互不相溶的液体分离的方法是分液,答案是分液;
(4)冷凝水从下口进入冷凝管,可以使整个冷凝管中充满水,提高冷凝效率,故从b口进、a口出。答案为b a;
(5)制取乙烯时,会发生副反应。浓硫酸有强氧化性,可以被还原为SO2气体,除去SO2可以选择NaOH溶液;温度如果没有迅速升高到170℃,会发生乙醇的分子间脱水生成乙醚。答案为氢氧化钠 乙醚。


 每课必练系列答案
每课必练系列答案科目:高中化学 来源: 题型:
【题目】请写出下列反应的化学方程式或离子方程式:
(1)钠在空气中燃烧:___;
(2)钠与水反应的离子方程式:___;
(3)碳酸钠转化为碳酸氢钠的化学方程式:___;
(4)碳酸氢钠溶液与氢氧化钠溶液反应的离子方程式:___;
(5)氯气和石灰乳反应化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白花丹酸具有镇咳祛痰的作用,其合成路线流程图如下:
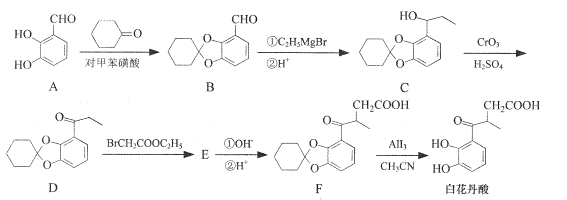
(1)A中的含氧官能团名称为__和_____。
(2)C-D的反应类型为 ___。
(3)白花丹酸分子中混有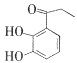 ,写出同时满足下列条件的该有机物的一种同分异构体的结构简式:____。
,写出同时满足下列条件的该有机物的一种同分异构体的结构简式:____。
①分子中有四种不同化学环境的氢;②与FeCl3溶液能发生显色反应,且1 mol该物质最多能与3 mol NaOH反应.
(4)E的结构简式为 ___。
(5)已知:![]() 根据已有知识并结合相关信息写出以
根据已有知识并结合相关信息写出以![]() 和CH3CH2OH为原料制备
和CH3CH2OH为原料制备![]() 的合成路线流程图(合成路线流程图示例见本题题干)____。
的合成路线流程图(合成路线流程图示例见本题题干)____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一定条件下,28.80g金属单质A与1.20molCl2完成反应,生成1.20molAClx,则x=__________,若A原子核内质子数等于中子数,则A原子核内中子数为__________ ,氯原子结构示意图为____________。
(2)现有氨气3.4g,在标准状况下其体积为____________,含有氮原子的数目为_____ ;将气体全部溶于水,配成500mL溶液,该溶液的物质的量浓度为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萜类化合物广泛存在于动植物体内,关于下列萜类化合物的说法正确的是( )

A. a和b都属于芳香族化合物
B. a和c分子中所有碳原子均处于同一平面上
C. a、b和c均能使酸性KMnO4溶液褪色
D. b和c均能与新制的Cu(OH)2反应生成红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是从海藻灰和智利硝石矿层中提取碘的主要反应:①2NaI+MnO2+3H2SO4===2NaHSO4+MnSO4+2H2O+I2 ;②2NaIO3+5NaHSO3===2Na2SO4+3NaHSO4+H2O+I2下列说法正确的是( )
A. 氧化性:MnO2>SO![]() >IO
>IO![]() >I2
>I2
B. I2在反应①中是还原产物,在反应②中是氧化产物
C. 反应①②中生成等量的I2时转移电子数之比为1∶5
D. NaHSO3溶液呈酸性,NaHSO3溶液中c(HSO![]() )>c(H2SO3)>c(SO
)>c(H2SO3)>c(SO![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式表达不正确的是 ( )
A. 向FeCl3溶液滴加HI溶液:2Fe3++2I-== 2Fe2++I2
B. CuSO4溶液吸收H2S 气体:Cu2++H2S == CuS↓+2H+
C. 用氢氧化钠溶液吸收工业废气中的NO2:2NO2+2OH- == NO![]() +NO
+NO![]() +H2O
+H2O
D. 向NH4Al(SO4)2溶液中滴加少量Ba(OH)2溶液:2NH4++Ba2++SO42-+2OH—= BaSO4↓+2NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某盐是一种重要的化工原料,在印染、制革、木材和农业等领域有重要用途,其溶液可能含有NH![]() 、Al3+、SO
、Al3+、SO![]() 、Fe2+、Cl-等若干种离子,某同学设计并完成了如下实验:
、Fe2+、Cl-等若干种离子,某同学设计并完成了如下实验:
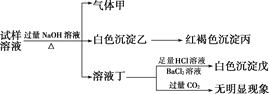
根据以上的实验操作与现象,该同学得出的结论不正确的是( )
A. 试样溶液中肯定有NH![]() 、SO
、SO![]() 和Fe2+
和Fe2+
B. 试样溶液中一定没有Al3+
C. 若气体甲在标准状况下体积为0.448 L,沉淀丙和沉淀戊分别为1.07 g和4.66 g,则可判断试样溶液中还有Cl-
D. 该盐在工业上可以用作净水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有CaCl2、MgCl2、Na2SO4以及泥沙等杂质,以下是制备精盐的实验方案,步骤如下图:
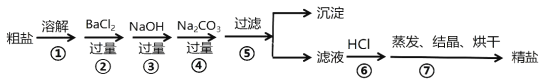
(1)第②步操作的目的是除去粗盐中的______________;( 填化学式,下同)
(2)图中“沉淀”的成分是:____________、_____________、____________、_____________;
(3)第④步操作的目的是除去________________、_________________;写出相应的离子反应方程式:_______________________;_________________________;
(4)第⑥步操作的目的是_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com