
工业上制取ClO2的化学反应:2NaClO3 + SO2 + H2SO4 = 2ClO2 + 2NaHSO4,下列说法正确的是( )
A.SO2在反应中被还原 B.NaClO3在反应中失去电子
C.H2SO4 在反应中作氧化剂 D.1mol氧化剂在反应中得到1mol电子
 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:
研究性学习小组做铜与浓硫酸反应的实验时,发现试管底部有白色固体并夹杂有少量黑色物质。倒去试管中的浓硫酸,将剩余固体(含少量浓硫酸)倒入盛有少量水的烧杯中,发现所得溶液为蓝色,黑色固体未溶解。过滤、洗涤后,向黑色固体中加入过量浓硝酸,黑色固体溶解,溶液呈蓝色,向所得溶液中加BaCl2溶液后有白色沉淀生成。下列结论不正确的是 ( )
A.铜与浓硫酸反应所得白色固体是CuSO4
B.加BaCl2溶液后所得白色沉淀是BaSO4
C.白色 固体中夹杂的少量黑色物质可能是CuO
固体中夹杂的少量黑色物质可能是CuO
D.白色固体中夹杂的少量黑色物质中含元素Cu、S
查看答案和解析>>
科目:高中化学 来源: 题型:
某烃1mol 最多能和2molHBr 加成反应,其所得的产物又能跟8molBr2 发生取代反应,最后得到一种只含碳、溴两种元素的化合物,则原烃为 ( )
A.C2H2 B.C3H4 C.C3H6 D.C4H6
查看答案和解析>>
科目:高中化学 来源: 题型:
由短周期元素构成的某离子化合物X中,一个阳离子和一个阴离子核外电子数之和为20,则有关X的下列说法中正确的是( )
A.X中阳离子和阴离子个数不一定相等
B.X中一定有离子键,一定不含共价键
C.若X只含两种元素,则这两种元素可在同一周期也可在同一主族
D.X中阳离子半径一定大于阴离子半径
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ |
(1)在这些元素中,金属性最强的元素是 ,最活泼的非金属元素是 ;
化学性质最不活泼的是: ;
在⑤~⑧元素中原子半径最小的是 ;(填元素符号)。
(2) 在最高价氧化物的水化物中,酸性最强的化合物是 ,碱性最强的
化合物 ,呈两性的氢氧化物是 ;(填化学式)
(3) 比较②、③对应氢化物的稳定性: > (用化学式表示)
(4)表示⑧与⑩的化合物的电子式 ,
该化合物含的化学键类型是 。(填“离子键”或“共价键”)
(5)写出⑧的单质与⑤的最高价氧化物的水化物的溶液反应的离子方程式:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
CH4、H2、CO的燃烧热分别为890.31 kJ/mol、285.8 kJ/mol、110.5 kJ/mol,下列热化学方程式书写正确的是( )
A.CH4(g)+2O2(g)===CO2(g)+2H2O(g)
ΔH=-890.31 kJ/mol
B.2H2(g)+O2(g)===2H2O(l)
ΔH=-285.8 kJ/mol
C.CO(g)+H2O(g)===CO2(g)+H2(g)
ΔH=+175.3 kJ/mol
D.2CO(g)+O2(g)===2CO2(g)
ΔH=-221 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
| 温度/℃ | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
(1)①写出工业合成氨的化学方程式:________________。
②由表中数据可知该反应为放热反应,理由是________。
③理论上,为了增大平衡时H2的转化率,可采取的措施是______
(填字母序号)。
a.增大压强
b.使用合适的催化剂
c.升高温度
d.及时分离出产物中的NH3
(2)原料气H2可通过反应CH4(g)+H2O(g)CO(g)+3H2(g)获取,已知该反应中,当初始混合气中的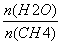 恒定时,温度、压强对平衡混合气中CH4含量的影响如图所示:
恒定时,温度、压强对平衡混合气中CH4含量的影响如图所示:
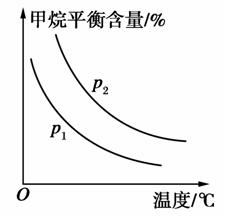
①图中,两条曲线表示压强的关系是p1________p2(填“>”、“=”或“<”)。
②该反应为________反应(填“吸热”或“放热”)。
(3)原料气H2还可通过反应CO(g)+H2O(g)CO2(g)+H2(g)获取。
①T ℃时,向容积固定为5 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO的浓度为0.08 mol·L-1,则平衡时CO的转化率为________该温度下反应的平衡常数K值为________。
②保持温度仍为T ℃,改变水蒸气和CO的初始物质的量之比,充入容积固定为5 L的容器中进行反应,下列描述能够说明体系处于平衡状态的是________________(填字母序号)。
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n(CO)n(H2O)n(CO2)n(H2)=11666
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com