
【题目】北京奥运会祥云火炬将中国传统文化、奥运精神及现代科技融为一体,火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.试回答下列问题: 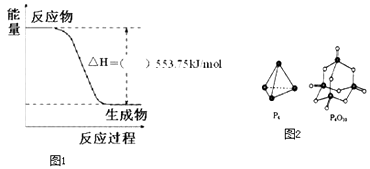
(1)如图1是一定量丙烷完全燃烧生成CO2和1mol H2O(l)过程中的能量变化图,(图中的括号内填入“+”或“﹣”).
写出表示丙烷燃烧热的热化学方程式:
(2)甲醇是一种清洁燃料,甲醇的燃烧热为726.51kJ/mol,若1mol甲醇和丙烷的混合物完全燃烧生成CO2和液态水共放出热量2498.4KJ,则混合物中甲醇和丙烷的物质的量之比为 .
(3)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式 .
(4)已知断裂下列化学键需要吸收的能量分别为P﹣P:akJmol﹣1、P﹣O:bkJmol﹣1、P=O:ckJmol﹣1、O=O:dkJmol﹣1 . 根据如图2所示的分子结构和有关数据估算反应:P4(s)+5O2(g)=P4O10(s)的△H=kJmol﹣1 .
【答案】
(1)C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H1=﹣2215.0 kJ/mol
(2)1:4
(3)NaOH(aq)+ ![]() H2SO4(aq)=
H2SO4(aq)= ![]() Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol
Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol
(4)解:各化学键键能为P﹣P a kJmol﹣1、P﹣O b kJmol﹣1、P=O c kJmol﹣1、O=O d kJmol﹣1,
反应热△H=反应物总键能﹣生成物总键能,
所以反应P4+5O2=P4O10的反应热△H=6akJmol﹣1+5dkJmol﹣1﹣(4ckJmol﹣1+12bkJmol﹣1)=(6a+5d﹣4c﹣12b)kJmol﹣1,答:△H为(6a+5d﹣12b﹣4c)kJmol﹣1
【解析】解:①图像是一定量丙烷完全燃烧生成CO2和1mol H2O(l)过程中的能量变化图,丙烷燃烧反应放热△H=﹣553.75KJ/mol;丙烷完全燃烧生成CO2和1mol H2O(l)过程中的能量变化图,反应放热△H=﹣553.75KJ/mol;则写出的热化学方程式为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H1=﹣2215.0 kJ/mol,所以答案是:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H1=﹣2215.0 kJ/mol;(2)若1mol甲醇和丙烷的混合物完全燃烧生成CO2和液态水共放出热量2498.4KJ,设1mol混合气体中甲醇物质的量x,丙烷物质的量为1﹣x,C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H1=﹣2215.0 kJ/mol,得到丙烷燃烧放热(1﹣x)2215KJ;依据条件得到:2498.4KJ﹣726.51xKJ=(1﹣x)2215KJ,计算得到x=0.2,则混合丙烷物质的量为0.8mol,则混合气体中丙烷和二甲醚物质的量之比=0.2:0.8=1:4,所以答案是:1:4;(3)1mol H2SO4溶液与足量 NaOH溶液完全反应,放出114.6kJ的热量,即生成2mol水放出114.6kJ的热量,反应的反应热为﹣114.6kJ/mol,
中和热为﹣57.3kJ/mol,则中和热的热化学方程式:NaOH(aq)+ ![]() H2SO4(aq)=
H2SO4(aq)= ![]() Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol,
Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol,
所以答案是:NaOH(aq)+ ![]() H2SO4(aq)=
H2SO4(aq)= ![]() Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol;
Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol;


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
A.9g甲基(﹣CH3)所含有的电子数是10 NA个
B.22.4L乙烷中含有的共价键数为7NA个
C.常温下,14g乙烯和丙烯的混合物中总原子数为3NA个
D.4.2g C3H6中含有的碳碳双键数一定为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知一定条件下A、B、C、D之间的转化关系如右图所示。下列说法正确的是
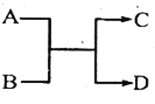
A. 若A为Fe,D为氢气,则B一定为酸
B. 若A、D为化合物,B为水,则C一定是气体单质
C. 若A、B、C、D均为化合物,该反应一定属于复分解反应
D. 若A、B、C、D均为10电子微粒(分子或离子),且C是可使湿润的红色石蕊试纸变蓝的气体,则D常温下一定呈液态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 已知氧化性Fe3+>I2,则FeCl2 溶液中滴加碘水: 2Fe2++I2=2Fe3++2I-
B. 向碳酸氢铵溶液中滴加过量热的氢氧化钠溶液NH4++HCO3-+2OH-![]() NH3↑+CO32-+2H2O
NH3↑+CO32-+2H2O
C. 向盐酸中滴加氨水: H++OH-= H2O
D. 铜溶于稀硝酸: Cu+4H++NO3-=Cu2++NO↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将15.6g Na2O2和5.4g Al同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72L,若反应过程中溶液的体积保持不变,则下列说法正确中缓慢通入标准状况下的HCl气体6.72L,若反应过程中溶液的体积保持不变,则下列说法正确的是( )
A. 标准状况下,反应过程中得到6.72L的气体
B. 最终得到的溶液中c(Na+)=c(Cl-)+c(OH-)
C. 最终得到7.8g的沉淀
D. 最终得到的溶液中c(Na+)=1.5mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理知识研究如何利用CO、SO2等污染物有重要意义.
(1)用CO可以合成甲醇.已知:
①CH3OH(g)+ ![]() O2(g)=CO2(g)+2H2O(l)△H=﹣764.5 kJmol﹣1
O2(g)=CO2(g)+2H2O(l)△H=﹣764.5 kJmol﹣1
②CO(g)+ ![]() O2(g)=CO2(g)△H=﹣283.0 kJmol﹣1
O2(g)=CO2(g)△H=﹣283.0 kJmol﹣1
③H2(g)+ ![]() O2(g)=H2O(l)△H=﹣285.8 kJmol﹣1
O2(g)=H2O(l)△H=﹣285.8 kJmol﹣1
则CO(g)+2H2(g)CH3OH(g)△H=kJmol﹣1
下列措施中能够增大上述合成甲醇反应的反应速率的是(填写序号).
a.使用高效催化剂 b.降低反应温度
c.增大体系压强 d.不断将CH3OH从反应混合物中分离出来
(2)在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2 , 在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图1所示. 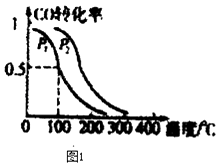
①p1p2(填“大于”、“小于”或“等于”);
②100℃时,该反应的化学平衡常数K=;
③100℃时,达到平衡后,保持压强P1不变的情况下,向容器中通入CO、H2号 CH3OH各0.5amol,则平衡(填“向右”、“向左”或“不”移动)
④在其它条件不变的情况下,再增加a mol CO和2a molH2 , 达到新平衡时,CO的转化率(填“增大”、“减小”或“不变”).
(3)在容积均为1L的密闭容器(a、b、c、d、e)中,分别充入1molCO和2molH2等量混合气体,在不同的温度下(温度分别为T1、T2、T3、T4、T5),经相同的时间,在t时刻,测得容器甲醇的体积分数如图所示.在T1﹣T2及T4﹣T5两个温度区间,容器内甲醇的体积分数的变化趋势如图2所示,其原因是 . 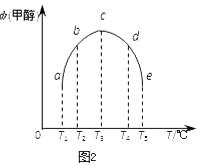
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料。工业上可用电子工业中刻蚀线路板的酸性废液(主要成分有FeCl3、CuCl2、FeCl2)制备,其制备过程如下:

查阅资料知,通过调节溶液的酸碱度可使Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
开始沉淀pH | 6.0 | 7.5 | 1.4 |
沉淀完全pH | 13 | 14 | 3.7 |
(1)氯酸钠的作用是__________。
(2)调节反应A的pH范围为__________,可以选择的试剂是__________(填序号)。
a.氨水 b.硫酸铜 c.氢氧化铜 d.碳酸铜
(3)反应B的温度要控制在60℃左右,且保持恒温,可采用的加热方法是__________。
(4)已知滤液中含有碳酸氢纳,写出生成碱式碳酸铜的离子方程式:__________。
(5)过滤得到的产品洗涤时,如何判断产品已经洗净__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯亚砜(SOCl2)是一种无色易挥发液体,遇水剧烈水解生成两种气体,常用作脱水剂,其熔点为-105℃,沸点为79℃,140℃以上时易分解。
(1)写出SOCl2吸收水蒸气的化学方程式:_________________
(2)甲同学设计如图所示装置,用ZnCl2·xH2O晶体制取无水ZnCl2、回收SOCl2并验证生成物中含有SO2(夹持及加热装置略)。

①装置的连接顺序为A→B→______→_____→_____。(填字母)
②冷凝管的作用是____________。
③实验结束后,为检测ZnCl2·xH2O晶体是否完全脱水,称取蒸干后的固体ag溶于水,加入足量稀硝酸和硝酸银溶液,过滤、冼绦、干燥,称得固体为bg。若![]() =___ (精确至0.1),即可证明ZnCl2·xH2O晶体已完全脱水。
=___ (精确至0.1),即可证明ZnCl2·xH2O晶体已完全脱水。
(3)乙同学认为SOCl2还可用作由FeCl3·6H2O制取无水FeCl3的脱水剂,但丙同学认为该实验中会发生氧化还原反应。请你设计并简述实验方案判断丙同学的观点:____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com