
分析 该有机化合物对氢气的相对密度是53,则相对分子质量为106,10.6g有机化合物A的物质的量为0.1mol,得到0.8molCO2气体和9.0g H2O,可知1mol有机物含有8molC原子,且n(H2O)=$\frac{9.0g}{18g/mol}$=0.5mol,n(H)=1mol,则1mol有机物含有10molH,且8×12+10=106,说明不含O元素,分子式为C8H10,以此解答该题.
解答 解:(1)该有机化合物对氢气的相对密度是53,则相对分子质量为106,
答:该有机物的相对分子质量为106;
(2)10.6g有机化合物A的物质的量为0.1mol,得到0.8molCO2气体和9.0g H2O,可知1mol有机物含有8molC原子,且n(H2O)=$\frac{9.0g}{18g/mol}$=0.5mol,n(H)=1mol,则1mol有机物含有10molH,且8×12+10=106,说明不含O元素,分子式为C8H10,
答:该有机物的分子式为C8H10;
(3)①分子中含有苯环,②它能使KMnO4酸性溶液褪色,则苯环上含有烃基,③它能发生硝化反应,当引入1个硝基时,只能得到1种硝基化合物,说明结构对称,应为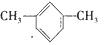 ,
,
答:该有机物的结构简式为 .
.
点评 本题考查有机物推断,为高频考点,侧重于学生的分析、计算能力的考查,注意把握有机物的结构与性质的关系,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 2mol气态H2与1mol气态氧气完全燃烧生成2mol液态水时放出571.6 kJ的热量 | |
| B. | 1mol气态H2与0.5mol气态氧气完全燃烧生成1mol液态水时吸收285.8kJ的热量 | |
| C. | 2个氢分子完全燃烧生成液态水时放出571.6 kJ的热量 | |
| D. | 上述热化学方程式可表示为H2(g)+O2(g)=H2O(1),H=-285.8 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
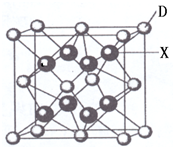 已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、B、C是同一周期的非金属元素.化合物DC 2的晶体为离子晶体,其阳离子与阴离子的个数比为1:1,D的二价阳离子比C的简单阴离子多一个电子层.AC 2为非极性分子.B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E原子序数为26.回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示).
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、B、C是同一周期的非金属元素.化合物DC 2的晶体为离子晶体,其阳离子与阴离子的个数比为1:1,D的二价阳离子比C的简单阴离子多一个电子层.AC 2为非极性分子.B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E原子序数为26.回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光导纤维应避免在强碱环境中使用 | |
| B. | 船体镀锌或镀锡均可保护船体,镀层破损后将立即失去保护作用 | |
| C. | 利用碳酸酯聚合材料生产一次性饭盒,可以减少对环境产生的白色污染 | |
| D. | 油脂皂化生成的高级脂肪酸钠是肥皂的有效成分 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | V2O5 | NH4VO3 | VOSO4 | (VO2)2SO4 |
| 溶解性 | 难溶 | 难溶 | 可溶 | 易溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫在氧气中燃烧,发出明亮的蓝紫色火焰,生成有刺激性气味的气体 | |
| B. | 碳在空气中燃烧,发出白光,生成使澄清石灰水变浑浊的气体 | |
| C. | 红磷在空气中燃烧,产生大量白色烟雾 | |
| D. | 将分别装有氨水和酚酞溶液的两只烧杯靠近,氨水先变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴加硫酸酸化的FeSO4溶液,平衡不移动 | |
| B. | 溶液颜色保持不变时,该反应达到平衡状态 | |
| C. | 滴加6 mol/L NaOH溶液,溶液颜色变深 | |
| D. | 平衡常数表达式为K=$\frac{2c(Cr{{O}_{4}}^{2-})•2c({H}^{+})}{c(C{r}_{2}{{O}_{7}}^{2-})•c({H}_{2}O)}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
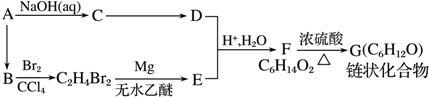
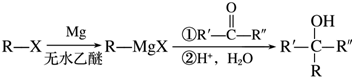 (R表示烃基,R′和R″表示烃基或氢)
(R表示烃基,R′和R″表示烃基或氢)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com