
A、 |
B、 |
C、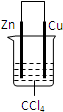 |
D、 |


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:

| 滴定序号 | 消耗KMnO4溶液体积(mL) |
| 1 | 19.98 |
| 2 | 20.02 |
| 3 | 19.12 |

查看答案和解析>>
科目:高中化学 来源: 题型:

| 化学反应 | 平衡常数 | 温度℃ | |
| 500 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②2H2(g)+CO2(g)?H2O+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g) | K3 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L H2中所含电子数为2NA |
| B、1mol CO2与1L 2mol?L-1的NaOH溶液反应后,溶液中CO32-数为NA |
| C、6.8 g熔融的KHSO4中含有0.1NA个阳离子 |
| D、3.36 L氯气与2.7 g铝充分反应,转移电子数一定为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性HClO4>H3PO4>HNO3>H2SiO4 |
| B、稳定性H2S>HCl>HBr>HI |
| C、还原性Rb>K>Na>Li |
| D、碱性Al(OH)3>Mg(OH)2>NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石灰乳与Na2CO3溶液混合:Ca2++CO32-═CaCO3↓ | ||||
B、用惰性电极电解氯化镁溶液:2Cl-+2H2O
| ||||
| C、将碳与足量的浓硫酸共热反应后的气体混合物,通入过量氢氧化钠溶液中:CO2+SO2+4OH-═SO32-+CO32-+2H2O | ||||
| D、漂粉精溶液滴入硫酸:Cl-+ClO-+2H+═Cl2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.OL 1.0mo1?L-1的Na2CO3水溶液中含有的氧原子数为3NA |
| B、25℃时pH=13的NaOH溶液中含有Na+的数目为0.1NA |
| C、28g晶体硅中含有化学键的个数为2NA |
| D、1mol的羟基与1mol的氢氧根离子所含电子数均为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素的种类由核内质子数决定 |
| B、原子的种类由核内质子数和中子数共同决定 |
| C、分子的种类由分子的组成决定 |
| D、原子的质量主要由原子核中质子和中子决定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-19 |
| AlAsO4 | 1.6×10-16 |
| FeAsO4 | 5.7×10-21 |
| 污染物 | H2SO4 | As |
| 浓度 | 28.42g/L | 1.6g?L-1 |
| 排放标准 | pH 6~9 | 0.5mg?L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com