
【题目】将1.12g铁粉加入25mL 2molL﹣1的氯化铁溶液中,充分反应后,其结果是( )
A. 铁有剩余,溶液呈浅绿色,Cl﹣浓度基本不变
B. 往溶液中滴入无色KSCN溶液,显黄色
C. Fe2+和Fe3+的物质的量之比为6:1
D. 氧化产物与还原产物的物质的量之比为2:5
【答案】B
【解析】铁粉的物质的量n=![]() =
=![]() =0.02mol,氯化铁的物质的量n=c×V=2molL-1×0.025L=0.05mol;铁粉与氯化铁的离子反应方程式为:Fe+2Fe3+=3Fe2+, 0.02mol铁粉完全反应需要0.04mol氯化铁。A.由于氯化铁剩余了0.01mol,铁完全反应,故A错误;B.氯化铁剩余,向溶液中滴入无色KSCN溶液,显血红色,故B错误;C.Fe2+的物质的量为0.06mol,氯化铁的物质的量为0.01mol,所以Fe2+和Fe3+的物质的量之比为6:1,故C正确;D.离子反应方程式为:Fe+2Fe3+=3Fe2+,由方程式可知氧化产物与还原产物的物质的量之比是 1:2,故D错误;故选C。
=0.02mol,氯化铁的物质的量n=c×V=2molL-1×0.025L=0.05mol;铁粉与氯化铁的离子反应方程式为:Fe+2Fe3+=3Fe2+, 0.02mol铁粉完全反应需要0.04mol氯化铁。A.由于氯化铁剩余了0.01mol,铁完全反应,故A错误;B.氯化铁剩余,向溶液中滴入无色KSCN溶液,显血红色,故B错误;C.Fe2+的物质的量为0.06mol,氯化铁的物质的量为0.01mol,所以Fe2+和Fe3+的物质的量之比为6:1,故C正确;D.离子反应方程式为:Fe+2Fe3+=3Fe2+,由方程式可知氧化产物与还原产物的物质的量之比是 1:2,故D错误;故选C。


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
【题目】(1)某简单离子的结构示意图可表示为:
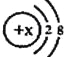
当x=8时,该粒子符号为_______;当x=11时,该粒子符号为_______;当x=13时,写出该粒子的硝酸盐的化学式为:__________。
(2)在一定温度下,向15g蒸馏水加入无水硫酸铜粉末,充分搅拌并过滤,得到一定质量的蓝色五水合硫酸铜晶体和8.4g滤液,若此温度下无水硫酸铜的溶解度为40g,则此无水硫酸铜的质量是________。
(3)已知难溶的物质在一定条件下可转化成更难溶的物质。在成有氯化银沉淀的试管中加入碘化钾溶液,振荡后可观察到白色沉淀逐渐变为黄色沉淀。请写出反应的化学方程式并简述理由。__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是( )
A.HCl和NaOH反应的中和热△H=-57.3kJ/mol,
则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol
B.CO的标准燃烧热是△H=-283.0KJ/mol,
则反应CO(g)+![]() O2(g)═CO2(g)的△H=﹣283.0KJ/mol
O2(g)═CO2(g)的△H=﹣283.0KJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1 mol硫燃烧生成气态三氧化硫所放出的热量是硫黄的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某班同学用如下实验探究Na2CO3、NaHCO3的性质。回答下列问题:
(1)甲组同学分别取1.0g Na2CO3、NaHCO3固体,各滴加几滴水,发现盛Na2CO3的试管温度上升,而盛NaHCO3的试管温度下降;原因是______________。
(2)乙组同学分别取0.1mol/L Na2CO3、0.1mol/LNaHCO3的溶液,用0.1mol/LHCl溶液滴定,pH变化与盐酸体积的关系如图所示:
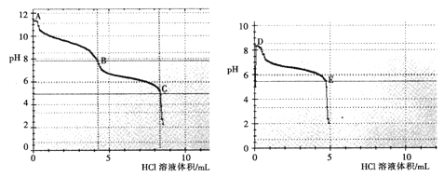
碳酸钠与盐酸反应pH有两次突变,达到两次反应终点,分别是__________(填A、B、C、D或E)。
B点的主要溶质是_____________(用化学式表示)。
③ B点__________(填“大于”或“小于”) D点的pH,主要原因是________________。
(3)丙组同学预测NaHCO3有酸性,向其溶液加入镁粉,发现有气泡和沉淀生成,写出化学方程式:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关右图装置的叙述中,正确的是( )
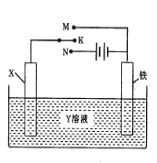
A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为外接电源的阴极保护法
B.若X为碳棒,Y为饱和NaOH溶液,开关K置于N处,保持温度不变,则溶液的pH保持不变
C.若X为银棒,Y为硝酸银溶液,开关K置于N处,铁棒质量将增加,溶液中银离子浓度将减小
D.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铁电极移动[来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.向密闭容器中通入0.1molN2和0.3molH2,在一定条件下充分反应,容器中N原子数为0.2NA
B.Cu-Zn-CuSO4原电池工作时,当转移电子数为0.2NA时,正极溶解Zn6.5g
C.电解102g熔融的Al2O3,能产生54g金属铝和33.6LO2,转移电子数为6NA
D.电解精炼铜当转移电子数为2NA时,阳极溶解的铜和阴极析出的铜均为64g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应中的能量变化,表述正确的是( )
A.放热反应中,反应物的总能量大于生成物的总能量
B.断开化学键的过程会放出能量
C.加热才能发生的反应一定是吸热反应
D.氧化反应均为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察下列几个装置示意图,有关叙述正确的是 ( )

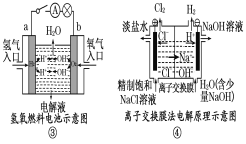
A.装置①中阳极上析出红色固体
B.装置②的待镀铁制品应与电源负极相连
C.装置③中外电路电子由a极流向b极
D.装置④的阳极反应为:2H+ + 2e— = H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是一种重要的基本化工原料,以它为原料还可以合成很多的化工产品。现有以下转化:

(1)聚乙烯的结构简式为 ;
(2)写出以下反应的化学方程式和反应类型:
② ,反应类型是
③ ,反应类型是
(3)实验室用如图装置制备乙酸乙酯:试管中碎瓷片的作用是 ;导管a的作用是导气和 ;试管b内饱和Na2CO3溶液的作用一方面是除去乙酸乙酯中混有的乙酸和乙醇,另一方面是 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com