
分析 (1)pH为12的NaOH溶液100mL中氢氧根离子浓度c(H+)=10-12mol/L,c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-12}}$=10-2mol/L,结合n=cV=$\frac{m}{M}$计算氢氧化钠质量;
(2)该溶液中水电离出的OH-浓度和水电离出氢离子浓度相同;
(3)先根据溶液的pH计算氢氧根离子浓度,再根据c1V1=c2(V1+V2)计算加入的水体积;
(4)先计算混合溶液中氢氧根离子浓度,再根据c(OH-)=$\frac{n(碱)-n(酸)}{V(碱)+V(酸)}$计算.
解答 解:(1)pH为12的NaOH溶液100mL中氢离子浓度c(H+)=10-12mol/L,c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-12}}$=10-2mol/L,需要氢氧化钠物质的量=10-2mol/L×0.1L=0.001mol,氢氧化钠溶质质量=0.001mol×40g/mol=0.04g,
故答案为:0.04;
(2)pH为12的NaOH溶液100mL中氢离子浓度c(H+)水=10-12mol/L=c(OH-)水,故该溶液中水电离出的OH-浓度为10-12mol/L,
故答案为:10-12;
(3)pH=12 的NaOH溶液中氢氧根离子浓度是0.01mol/L,pH=11的氢氧化钠溶液中氢氧根离子浓度是0.001mol/L,设加入水的体积是V2,c1V1=c2(V1+V2)=0.01mol/L×0.1L=(0.1+V2)L×0.001mol/L,则:V2=$\frac{0.01mol×0.1L}{0.001mol/L}$-0.1L=0.9L=900mL,
故答案为:900;
(4)盐酸的浓度是0.1mol/L,要使它的pH降到11,设加入盐酸的体积是V,c(OH-)=$\frac{n(碱)-n(酸)}{V(碱)+V(酸)}$=$\frac{0.01mol/L×0.1L-0.1mol/L×VL}{0.1L+VL}$=0.001mol/L,
解得:V=8.18mL,
故答案为:8.18.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算,题目难度中等,明确溶液pH的计算方法为解答关键,试题侧重考查学生达到分析、理解能力及化学计算计算能力.


科目:高中化学 来源: 题型:多选题
| A. | 以非极性键结合起来的双原子分子一定是非极性分子 | |
| B. | 在所有分子中都存在化学键 | |
| C. | σ键一定比π键强度大 | |
| D. | s-s σ键与p-p σ键的电子云形状对称性不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol任何物质体积的大小取决于构成物质的粒子的大小和粒子之间的距离 | |
| B. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| C. | 蒸馏中,冷却水应从冷凝管的下口通入,上口流出 | |
| D. | 蒸馏时,温度计水银球应浸没在液体中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 28g乙烯和环丁烷(C4H8)的混合气体含有的碳原子数为2NA | |
| B. | 标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为$\frac{7}{22.4}$NA | |
| C. | 1 mol甲基(-CH3)所含的电子总数为9NA | |
| D. | 0.5 mol 1,3-丁二烯分子中含有C=C双键数为 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 分子式为C16H18O9 | |
| B. | 1mol咖啡鞣酸水解时可消耗8mol NaOH | |
| C. | 1mol 咖啡鞣酸最多可消耗Br2 6 mol | |
| D. | 能发生取代反应和加成反应,但不能消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3He与3H中含有相同的中子数 | |
| B. | 通过化学反应可以实现3He与4He的相互转化 | |
| C. | 1 mol氦气含有质子数为2 mol | |
| D. | 3He与4He互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
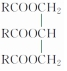 ”来表示,其中R为碳原子数目多于10的链烃基,可以相同也可以不同.分子式为C51H92O6的某油脂在稀硫酸中加热水解后得到A、B两种物质,若A的相对分子质量为92(已知:R1-CH═CH-R2$→_{H+}^{KMnO_{4}}$R1-COOH+R2-COOH),则
”来表示,其中R为碳原子数目多于10的链烃基,可以相同也可以不同.分子式为C51H92O6的某油脂在稀硫酸中加热水解后得到A、B两种物质,若A的相对分子质量为92(已知:R1-CH═CH-R2$→_{H+}^{KMnO_{4}}$R1-COOH+R2-COOH),则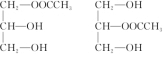 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
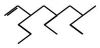 命名正确的是( )
命名正确的是( )| A. | 5,7-二甲基-3-乙基-1-辛烯 | B. | 3-乙基-5,7-二甲基-1-壬烯 | ||
| C. | 3-甲基-5-乙基-7-丙基-8-壬烯 | D. | 7-甲基-5-乙基-3-丙基-1-壬烯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com