
在常温下,下列各物质能使酸性KMnO4溶液褪色又能使溴水褪色并且化学反应原理相同的是( )
A.SO2 B.CH2=CH2 C. D.CH4
科目:高中化学 来源: 题型:
将煤焦油中的苯、甲苯和苯酚进行分离,可采取如图所示的方法和操作:
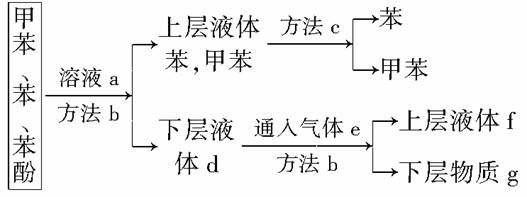
(1)写出物质a和e的分子式:a________;e________。
(2)写出分离方法b和c的名称:b________;c________。
(3)混合物中加入溶液a后反应的化学方程式__________________
__________________________________________________________;
分离出的苯酚含在________中。
查看答案和解析>>
科目:高中化学 来源: 题型:
1,2 -二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2 -二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。

填写下列空白:
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式。_ ; 。
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象:____________________________________________。
(3)容器c中NaOH溶液的作用是:________________________________________。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因: _____, _____。
查看答案和解析>>
科目:高中化学 来源: 题型:
海水是巨大的化学资源库,下列有关海水综合利用说法正确的是( )
A.从海水中可以得到NaCl,电解熔融NaCl可制备金属Na
B.海水蒸发制海盐的过程中只发生了化学变化
C.海水的淡化,只需经过化学变化就可以得到
D.利用海水、铝、空气的航标灯的原理是将电能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列有关说法正确的是( )

A.洗气瓶中产生的沉淀是碳酸钡 B.洗气瓶中产生的沉淀是硫酸钡
C.在Z导管出来的气体中无二氧化碳 D.洗气瓶中产生的沉淀是碳酸钡和硫酸钡
查看答案和解析>>
科目:高中化学 来源: 题型:
某氮肥厂氨氮废水中氮元素多以 和NH3·H2O的形式存在,该废水的处理流程如下:
和NH3·H2O的形式存在,该废水的处理流程如下:


(1)过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30 ℃,通空气将氨赶出并回收。用离子方程式表示加NaOH溶液的作用
(2)过程Ⅱ:在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成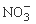 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:

第一步反应是 反应(选填“放热”或“吸热”),判断依据是
。1 mol  (aq)完全转化成
(aq)完全转化成 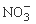 (aq)共与环境交换了 kJ热量。
(aq)共与环境交换了 kJ热量。
(3)过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 g CH3OH转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比是
查看答案和解析>>
科目:高中化学 来源: 题型:
下列A~I九种物质之间的转化关系如图所示,其中部分生成物或反应条件已略去。已知A在常温下为黑色固体单质,常温下C、E、F都是无色气体。

请回答下列问题:
(1)C的固体名称_______,F的化学式是________________________________。
(2)A与B反应的化学方程式是_______________________________________
________________________________________________________________________。
(3)G与H反应的离子方程式是____________________________________
________________________________________________________________________;
E转变为H和I的离子方程式是____________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向溴水中加入足量乙醛溶液,可以看到溴水褪色。对产生此现象的原因有如下三种猜想:①溴水与乙醛发生了取代反应;②溴水与乙醛发生了加成反应;③溴水将乙醛氧化成乙酸。为探究到底哪一种猜想正确,一研究性学习小组提出了如下两种方案:
方案一:检验褪色后溶液的酸碱性。
方案二:测定反应前溴水中Br2的物质的量和反应后Br-的物质的量。
(1)方案一是否可行?________,理由是________________。
(2)假设测得反应前溴水中Br2的物质的量为a mol。
①若测得反应后n(Br-)=________mol,说明溴水与乙醛发生了取代反应;
②若测得反应后n(Br-)=________mol,则说明溴水与乙醛发生了加成反应;
③若测得反应后n (Br-)=________mol,则说明溴水将乙醛氧化成乙酸。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com