
| A. | 在周期表中,元素的族序数都等于其原子的最外层电子数 | |
| B. | 周期表中非金属性最强的元素,其最高价氧化物的水化物酸性也最强 | |
| C. | 同主族元素随原子核电荷数的递增,原子半径依次减小 | |
| D. | ⅦA族元素的单质,随分子量的增大,熔、沸点升高;ⅠA族单质,随分子量的增大,熔、沸点降低 |
分析 A.主族元素的族序数=最外层电子数;
B.周期表中非金属性最强的元素是氟,而氟无正价;
C.同主族元素随原子核电荷数的递增,电子层数增多,原子半径依次增大;
D.周期表中,同一主族元素,金属单质的熔沸点逐渐降低,非金属单质的熔沸点逐渐升高.
解答 解:A.元素周期表中,主族元素的族序数=最外层电子数,副族、0族等没有此规律,故A错误;
B.元素的非金属性越强,对应的最高价氧化物对应的水化合物酸性越强,而非金属性最强的元素是氟,无正价,故B错误;
C.同主族元素随原子核电荷数的递增,电子层数增多,原子半径依次增大,故C错误;
D.第ⅦA族元素是卤互单质,都是分子晶体,随分子量的增大,熔、沸点逐渐升高;ⅠA族单质为碱金属元素(除H元素外),随分子量的增大,熔、沸点降低,故D正确;
故选D.
点评 本题考查元素周期表、元素周期律及非金属性比较的考查,题目难度不大,明确元素周期表结构、元素周期律内容我解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 离子的还原性强弱:I->Fe2+>Cl- | |
| B. | 当a>b时,发生的离子反应:2Fe2++Cl2═2Fe3++2Cl- | |
| C. | 当a=b时,发生的离子反应:2I-+Cl2═I2+2Cl- | |
| D. | 当3a≤2b时,发生的离子反应:2Fe2++4I-+3Cl2═2Fe3++2I2+6Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Cu、Ag分别作原电池两电极,AgNO3溶液作电解质溶液 | |
| B. | 用Ag作电解池的阳极,石墨作电解池的阴极,CuSO4溶液作电解质溶液 | |
| C. | 用Ag、C分别作原电池两电极,CuSO4溶液作电解质溶液 | |
| D. | 用Ag作电解池的阳极,石墨作电解池的阴极,AgNO3溶液作电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸滴在银片上:2Ag+2H+═2Ag++H2↑ | |
| B. | 碳酸钠与稀盐酸的反应:CO32-+2H+═H2O+CO2↑ | |
| C. | Mg(OH)2与盐酸的反应:H++OH-═H2O | |
| D. | 铜片放入ZnSO4溶液中:Cu+Zn2+═Cu2++Zn |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,0.5 mol•L-1 Fe2(SO4)3溶液中含Fe3+数目为1 NA | |
| B. | 标准状况下,22.4L苯中含C-H数目为6NA | |
| C. | 常温常压下,16g O2和O3混合气体中,含氧原子的总数为1NA | |
| D. | 5.6g Fe与足量稀盐酸反应,转移电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
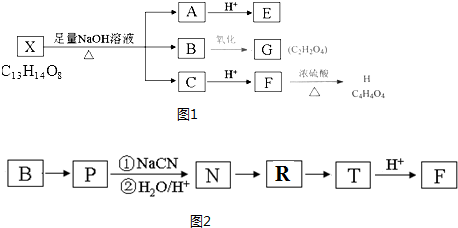
 +(2n-1)H2O.
+(2n-1)H2O.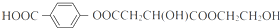 .
.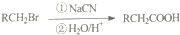
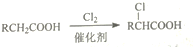

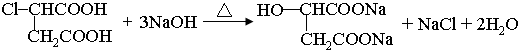 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
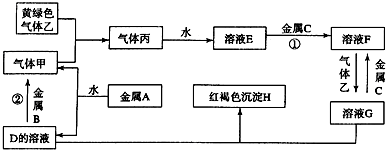
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com