
普罗加比对瘫痫、痉挛和运动失调均有良好的治
疗效果,其结构如下图所示,有关普罗加比的说法正确的是
A.该分子在1H核磁共振谱中有12个峰
B.久置在空气中的普罗加比会因氧化而变质
C.1 mol普罗加比最多可与3 mol NaOH反应
D.一定条件下,1mol普罗加比最多能与2mol H2发生加成反应
科目:高中化学 来源: 题型:
下列有关离子检验的操作和实验结论都正确的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入氯化钡溶液,有白色沉淀生成, 再加盐酸酸化,沉淀不溶解 | 该溶液中一定含有SO42- |
| B | 向某溶液中加入氨水,产生沉淀以后继续滴加氨水,沉淀溶解 | 该溶液中一定含有Al3+ |
| C | 向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色气体 | 该溶液中一定含有CO32- |
| D | 向某溶液中加BaCl2无沉淀产生,加盐酸产生能使澄清石灰水变浑浊的无色气体 | 该溶液中可能含有HCO3— |
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应Sn(s)+Pb2+(aq) Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是
A.往平衡体系中加入金属铅后,c(Pb2+)增大
B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变大
C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0
D.25℃时,该反应的平衡常数K=2.2

查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能获得成功的是( )
A.将乙醛滴入银氨溶液中,加热煮沸制银镜
B.苯与浓溴水反应制取溴苯
C.向浓溴水中加几滴苯酚,观察到有白色沉淀生成
D.1 mol/L CuSO4溶液2 mL和0 .5 mol/L NaOH溶液4 mL混合后加入40%的乙醛溶液0.5 mL,加热煮沸,观察沉淀的颜色
.5 mol/L NaOH溶液4 mL混合后加入40%的乙醛溶液0.5 mL,加热煮沸,观察沉淀的颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物X的分子式为C4H8O2,X在酸性条件下与水反应,生成两种有机物Y和Z,Y在铜催化下被氧化为W,W能发生银镜反应。
(1)X中所含的官能团是________(填名称)。
(2)写出符合题意的X的结构简式___________________________________________。
(3)若Y和Z含有相同的碳原子数,写出下列反应的化学方程式:Y与浓硫酸的混合物共热发生消去反应_________________________________________________________________。
W与新制Cu(OH)2反应______________________________________________。
(4)若X的某种同分异构体能使石蕊变红色,可能有________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
酚酯是近年高考有机化学命题的热点,其合成方法之一是由酚与酰卤(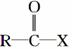 )反应制得。
)反应制得。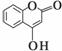
是一种医药中间体,常用来制备抗凝血药,可通过 下列路线合成:
下列路线合成:
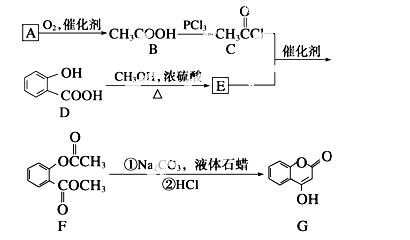
(1)A与银氨溶液反应有银镜生成,则A的结构简式是_______________________。
(2)B—→C的反应类型是______________。
(3)E的结构简式是______________________________________________________。
(4)写出F和过量NaOH溶液共热时反应的化学方程式:
______________________________________________________________________。
(5)下列关于G的说法正确的是__________(填序号)。
a.能与溴单质反应
b.能与金属钠反应
c.1 mol G最多能和3 mol氢气反应
d.分子式是C9H6O3
查看答案和解析>>
科目:高中化学 来源: 题型:
莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是
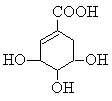 A.分子式为C7H6O5
A.分子式为C7H6O5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.在水溶液羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
乙二醇(C2H6O2)为常用的化工原料。淀粉通过下列转化可以得到乙二醇,A为一种单糖,B为一种有特殊香味的一元醇,C为一种气体 。回答下列问题:
。回答下列问题:
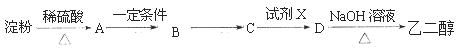
(1)A的名称为 ;A→B的化学反应方程式为 ;B→C的反应条件 ;
(2)试剂X为 ;D→乙二醇的反应类型为 。
(3)某同学想确认淀粉和稀硫酸是否已经发生反应,取反应混合液少许,加新制的碱性氢氧化铜悬浊液并加热,没有出现红色沉淀,能否说明反应未发生 (填“能”或“否”),为什么 。
查看答案和解析>>
科目:高中化学 来源: 题型:
阿司匹林(乙酰水杨酸)已应用百年,成为医药史上三大经典药物之一,至今它仍是世界上应用最广泛的解热、镇痛和抗炎药,也是作为比较和评价其他药物的标准制剂。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成该物质,设计的合成路线为:
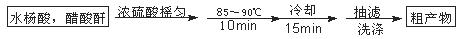
一、制备
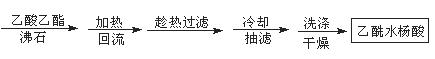
二、提纯
方案1

方案2
主要试剂和产品的物理常数
| 名 称 | 相对分子质量 | 熔点或沸点(0C) | 水 | 醇 | 醚 |
| 水杨酸 | 138 | 158(熔点) | 微溶 | 易溶 | 易溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 反应 | 可溶 | 易溶 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 | 可溶 | 微溶 |
请根据以上信息回答下列问题:
 (1)①合成阿斯匹林时,还会生成一些副产品,其中有一种是高分子,为了分离此物质,方案1中加入A物质为 溶液。
(1)①合成阿斯匹林时,还会生成一些副产品,其中有一种是高分子,为了分离此物质,方案1中加入A物质为 溶液。
②本方案抽滤 后进行洗涤,其具体操作是 。
后进行洗涤,其具体操作是 。
(2)方案2为改进的提纯方法,称为重结晶提纯法。
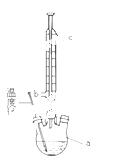
①步骤2回流的装置如图所示,写出仪器a的名称 ,使用温度计的目的是 ,冷凝水的流向为 。
②方案2所得产品的有机杂质要比方案1少的原因是 。
(3)该学习小组在实验中原料用量:2.0g水杨酸、5.0ml醋酸酐(ρ=1.08g·cm-3),最终称量产品m=2.2g ,则乙酰水杨酸的产率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com