
| ||
| 5g |
| 100g/mol |
| ||


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
A、聚四氟乙烯的结构简式: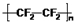 | ||
B、Na2O2的电子式: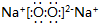 | ||
C、
 | ||
D、丙烷的分子球棍模型示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可能含有K+ |
| B、肯定含有NO3-、SO42-、NH4+、CO32- |
| C、一定不含有NO3- |
| D、一定含有K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| B、加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- |
| C、加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
| D、验证烧碱溶液中是否含有Cl-,先加稍过量的稀硝酸除去OH-,再加入AgNO3溶液,如有白色沉淀,则证明有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 部分结构知识 | 部分性质 |
| X | X原子核外电子占有9个原子轨道 | X的一种氧化物是形成酸雨的主要物质 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数等于2n-3 (n为原子核外电子层数) | 化学反应中Z原子易失去最外层电子形成Zn+ |
| W | W基态原子的外围电子排布式为3d64s2 | 高温下,W与水蒸气反应生成氢气和黑色氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com