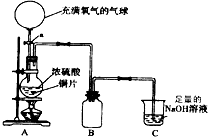
某中学高一课外兴趣小组为探究铜跟硫酸的反应情况,设计了如图所示装置进行有关实验.
(1)先关闭活塞a,将6.4g铜片和12mL某浓度的浓硫酸放在圆底烧瓶中共热至反应完毕,发现烧瓶中还有铜片剩余.再打开活塞a,将气球中的氧气缓缓挤入圆底烧瓶,最后铜片完全消失.
写出上述过程中烧瓶内发生的化学方程式:
关闭活塞a
Cu+2H
2SO
4(浓)
CuSO
4+SO
2↑+2H
2O
Cu+2H
2SO
4(浓)
CuSO
4+SO
2↑+2H
2O
;
打开活塞a
2Cu+O
2+2H
2SO
42CuSO
4+2H
2O (或分步写成:2Cu+O
2=2CuO;CuO+H
2SO
4=CuSO
4+H
2O也可)
2Cu+O
2+2H
2SO
42CuSO
4+2H
2O (或分步写成:2Cu+O
2=2CuO;CuO+H
2SO
4=CuSO
4+H
2O也可)
;
(2)该小组甲同学对“如何检验SO
2中混有少许CO
2”这个问题很感兴趣,他将A中铜片换作木炭粉,并在A、B之间连接了如下装置:
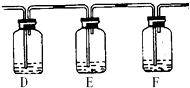
试剂:a.NaOH溶液 b.品红溶液 c.酸性KMnO
4溶液 d.Ca(OH)
2溶液
请回答:
①该同学的实验装置A中发生的化学方程式:
C+2H
2SO
4(浓)
CO
2↑+2SO
2↑+2H
2O
C+2H
2SO
4(浓)
CO
2↑+2SO
2↑+2H
2O
.
②若要达到此目的,可以在:(填所提供试剂编号)
D中加入
c
c
;E中加入
b
b
;F中加入
d
d
.
(3)事实证实,第(1)问铜片完全消失后,硫酸仍有剩余,乙同学欲测定余酸的物质的量浓度,假设反应前后溶液体积变化忽略不计,他向反应后溶液中加入含溶质a mol的NaOH溶液刚好使溶液中Cu
2+全部沉淀.据此,他能求出余酸的物质的量浓度吗?若能,请写出余酸物质的量浓度的表达式:
mol/L(用含a的代数式表达,若不能,该空不填).



 某中学高一课外兴趣小组为探究铜跟硫酸的反应情况,设计了如图所示装置进行有关实验.
某中学高一课外兴趣小组为探究铜跟硫酸的反应情况,设计了如图所示装置进行有关实验. 试剂:a.NaOH溶液 b.品红溶液 c.酸性KMnO4溶液 d.Ca(OH)2溶液
试剂:a.NaOH溶液 b.品红溶液 c.酸性KMnO4溶液 d.Ca(OH)2溶液 2CO2+4H2O则由此得出的下列结论,完全正确的一组是( )
2CO2+4H2O则由此得出的下列结论,完全正确的一组是( ) 2CO2+4H2O则由此得出的下列结论,完全正确的一组是
2CO2+4H2O则由此得出的下列结论,完全正确的一组是