
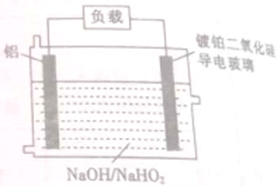
 镁、铝、硅均为第三周期元素,按要求回答下列问题:
镁、铝、硅均为第三周期元素,按要求回答下列问题:| 3 |
| 2 |


科目:高中化学 来源: 题型:
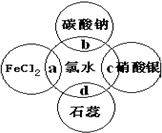 反应,且氯水足量).
反应,且氯水足量).查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH+HCl═NaCl+H2O | ||||
| B、Zn+2HCl═ZnCl2+H2↑ | ||||
C、MnO2+4HCl(浓)
| ||||
| D、CaCO3+2HCl═CaCl2+H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,8g O2含有0.5 NA个电子 |
| B、1mol?L-1 Ca(ClO)2溶液中含有ClO-的数目为2NA |
| C、标准状况下,22.4LHCl溶于1L水中所得的盐酸含有NA个HCl分子 |
| D、1molNa被完全氧化生成Na2O2失去NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
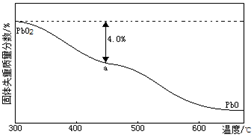 金属铅为带蓝色的银白色重金属,其单质及化合物可用于铅蓄电池、耐酸设备及X射线防护材料.回答下列问题:
金属铅为带蓝色的银白色重金属,其单质及化合物可用于铅蓄电池、耐酸设备及X射线防护材料.回答下列问题:| 放电 |
| 充电 |
| 样哦起始质量-a点固体质量 |
| 样品起始质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
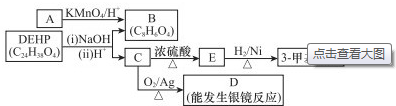
查看答案和解析>>
科目:高中化学 来源: 题型:
| 现象或操作 | 解释 | |||
| A | KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪去 | SO2具有漂白性 | ||
| B | 苯酚中滴加浓溴水酸性明显增强 | 可能发生了取代反应 | ||
| C | 某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 | 不能说明该溶液中一定含有SO
| ||
| D | 将SO2通入含HClO的溶液中,生成H2SO4, | HClO酸性比H2SO4强 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com