
| A. | 分子里含有碳碳三键的脂肪烃 | |
| B. | 易发生加成反应 | |
| C. | 既能使溴水褪色也能使酸性高锰酸钾溶液褪色 | |
| D. | 分子里所有的碳原子都处在同一条直线上 |
分析 结构中含有碳碳三键的脂肪烃为炔烃,由于碳碳三键是不饱和键,故能发生加成反应,且易被强氧化剂氧化,最简单的炔烃为乙炔,乙炔中的4个原子共直线,据此分析.
解答 解:A、结构中含有碳碳三键的脂肪烃为炔烃,故炔烃中碳碳三键为官能团,故A正确;
B、由于碳碳三键是不饱和键,故能和氢气、卤素单质和水等发生加成反应,故B正确;
C、炔烃中含碳碳三键,故能和溴水发生加成反应而使溴水褪色,且易被强氧化剂氧化,故能被高锰酸钾溶液氧化而使高锰酸钾溶液褪色,故C正确;
D、最简单的炔烃为乙炔,乙炔中的4个原子共直线,但并不是所有的炔烃中的碳原子都在一条直线上,故D错误.
故选D.
点评 本题考查了炔烃的结构和化学性质,难度不大,应注意的是炔烃使溴水和高锰酸钾溶液褪色,但原理不同.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
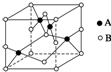 纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.回答下列问题:
纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2分子中,两个O之间形成2对共用电子对 | |
| B. | N2的电子式是N┇┇N | |
| C. | CO2和CS2都是直线型分子 | |
| D. | 白磷和甲烷都是正四面体型,键角都是109°28′ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
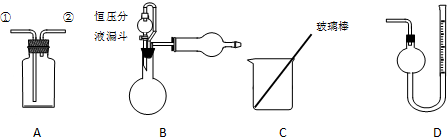
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冰的密度比液态水的密度小是因为冰分子之间含有较强的化学键 | |
| B. | 氨分子的键角比甲烷分子的键角小是因为两个分子中中心原子的杂化方式不同 | |
| C. | HF的沸点比HCl的沸点高是因为HF分子内含有氢键 | |
| D. | HF比HCl稳定是因为HF分子中共价键的键能大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
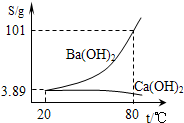 实验室有一份混有碳酸钙杂质的碳酸钡样品.分离并提纯碳酸钡的实验步骤如下,请根据要求填空(如图为Ba(OH)2和Ca(OH)2的溶解度曲线):
实验室有一份混有碳酸钙杂质的碳酸钡样品.分离并提纯碳酸钡的实验步骤如下,请根据要求填空(如图为Ba(OH)2和Ca(OH)2的溶解度曲线):查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,铝遇冷浓硝酸钝化 | B. | 浓盐酸的质量减轻 | ||
| C. | 澄清的石灰水变浑浊 | D. | 氢氧化钠固体发生潮解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
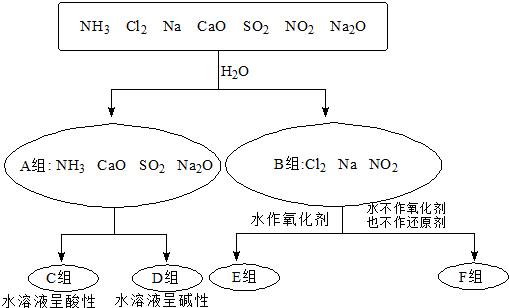
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com