
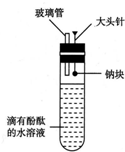
 有人设计了如图所示的实验装置,目的是做钠与水反应的实验并验证:
有人设计了如图所示的实验装置,目的是做钠与水反应的实验并验证:分析 (1)钠与水反应生成的NaOH能通过滴有酚酞的水溶液变红来检验,生成的H2则应该收集后再进行点燃实验,据此选择仪器;
(2)接下来的操作是让钠与水接触开始反应,并观察现象、收集和验证产生的气体是否是氢气;
(3)钠浮在水面上,很快熔化成闪亮的小球,并逐渐消失,水溶液由无色变成红色;反应有气体生成,点燃小试管中的气体时,有尖锐的爆鸣声;
(4)熔小球、浮水面说明本实验钠的物理性质有钠熔点低,密度比水小,溶液变红、生成气体爆鸣声,能证明钠与水反应生成的产物有生成氢氧化钠、氢气,
(5)钠与水反应生成氢氧化钠和氢气.
解答 解:(1)钠与水反应的化学方程式为:2Na+2H2O═2NaOH+H2↑,生成的NaOH能通过滴有酚酞的水溶液变红来检验,生成的H2则应该收集后再进行点燃实验,故还需要用到小试管和酒精灯,
故答案为:小试管和酒精灯;
(2)接下来的操作是让钠与水接触开始反应,并观察现象、收集和验证产生的气体是否是氢气,应该将大头针向上提,使钠块从针头脱落并落入水中,将小试管扣在导管上收集反应产生的气体,用拇指堵住试管口移近酒精灯,松开拇指点燃试管中的气体,
故答案为:将大头针向上抽,使钠块掉入水中,在玻璃管口处用小试管收集气体;
(3)钠浮在水面上,很快熔化成闪亮的小球,并逐渐消失,水溶液由无色变成红色;反应有气体生成,点燃小试管中的气体时,有尖锐的爆鸣声,
故答案为:金属钠熔成小球,浮在水面上游动,溶液变成红色,将已收集了气体的小试管靠近火焰时发出爆鸣声;
(4)熔小球、浮水面说明本实验钠的物理性质有钠熔点低,密度比水小,溶液变红、生成气体爆鸣声能证明钠与水反应生成的产物有生成氢氧化钠、氢气,
故答案为:熔点低,密度比水小;氢氧化钠、氢气;
(5)钠与水反应生成氢氧化钠和氢气,2Na+2H2O═2Na++2OH-+H2↑,
故答案为:2Na+2H2O═2Na++2OH-+H2↑.
点评 本题考查钠与水反应的知识,主要是反应现象和原因,产物的实验验证,掌握基础是解题关键,题目较简单.


 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 | |
| B. | 具有相同通式的有机物不一定互为同系物 | |
| C. | 含有相同官能团,且相对分子量相差14的有机物一定互为同系物 | |
| D. | 互为同系物的有机物,其化学性质相似 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
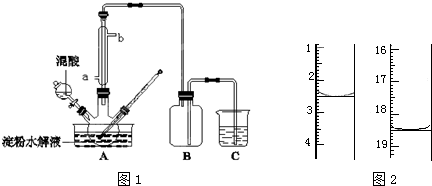
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生活中常用热的小苏打去污,利用了水解吸热的特点 | |
| B. | Mg可由电解MgCl2水溶液制取,Al可由电解熔融Al2O3制取 | |
| C. | 少数商贩在蔬菜表面洒少许福尔马林,可延长保鲜时间 | |
| D. | SiO2可用来制作光导纤维,但SiO2本身不导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
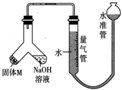 某课外兴趣小组为探究某种铝合金(合金元素为Mg、Al)是否符合国家质量标准(国家规定其中铝含量不能低于78%),设计如图所示装置进行实验.
某课外兴趣小组为探究某种铝合金(合金元素为Mg、Al)是否符合国家质量标准(国家规定其中铝含量不能低于78%),设计如图所示装置进行实验.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
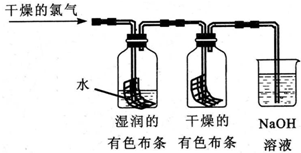
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
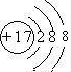 .
.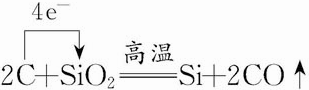 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
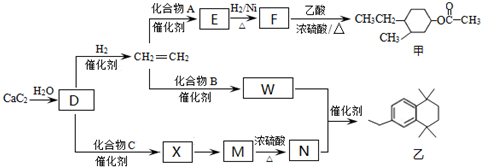
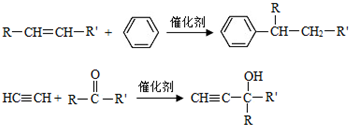 (-R、-R′代表烃基或-H)
(-R、-R′代表烃基或-H)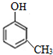 ,“E→F”的反应类型为加成反应.
,“E→F”的反应类型为加成反应.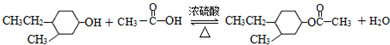 .
.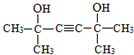 .
.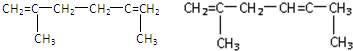 .
.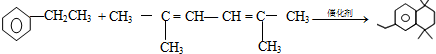 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com