
| A. | 在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解 | |
| B. | 可用加热氯化铵分解的方法制取氨气 | |
| C. | 在BaCl2溶液中通入SO2气体会产生白色沉淀 | |
| D. | 向某无色溶液中加入AgNO3溶液,产生白色沉淀,再加入稀盐酸,沉淀不消失,则该无色溶液中可能含有Cl- |
分析 A.酸性条件下,硝酸根离子与Cu发生氧化还原反应;
B.氯化铵分解后,在试管口氨气、HCl又化合生成氯化铵;
C.盐酸的酸性大于亚硫酸的酸性,BaCl2溶液中通入SO2气体不反应;
D.白色沉淀可为AgCl,不溶于酸.
解答 解:A.酸性条件下,硝酸根离子与Cu发生氧化还原反应,则再加入Cu(NO3)2固体,铜粉溶解,故A错误;
B.氯化铵分解后,在试管口氨气、HCl又化合生成氯化铵,则不能制备氨气,应选铵盐与碱加热制备,故B错误;
C.盐酸的酸性大于亚硫酸的酸性,BaCl2溶液中通入SO2气体不反应,则不会生成沉淀,故C错误;
D.白色沉淀可为AgCl,不溶于酸,则该无色溶液中可能含有Cl-,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、氧化还原反应、气体的制备、离子检验为解答的关键,侧重分析与实验能力的考查,注意实验与元素化合物知识的结合,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | NH4+、Ag+、PO43-、Cl- | B. | Al3+、H+、I-、HCO3- | ||
| C. | K+、Na+、NO3-、MnO4- | D. | Al3+、Mg2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CHO (l) | B. | CH3CHO (g) | C. | CO(g) | D. | CO2(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 试剂(或条件) | |
| A | 温度对H2O2分解反应速率的影响 | ①热水浴②冰水浴 |
| B | 用稀硫酸比较铝和铁的金属活动性 | ①铝粉 ②铁钉 |
| C | 用酸化的AgNO3溶液检验海水中Cl-能否蒸馏除去 | ①海水 ②蒸馏所得液体 |
| D | 用Na块检验乙醇分子存在不同于烃分子里的氢原子 | ①乙醇 ②煤油 |

| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
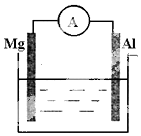 如图所示装置:
如图所示装置:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水 | B. | NaOH固体 | C. | Na2CO3固体 | D. | NaNO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com