
【题目】在一容积可变的密闭容器中加入WO3和H2进行反应:WO3(s)+3H2(g)![]() W(s)+3H2O(g),下列说法不正确的是( )
W(s)+3H2O(g),下列说法不正确的是( )
A.将容器的体积缩小一半,其反应速率增大
B.保持体积不变,充入氩气,其反应速率不变
C.保持压强不变,充入氖气,H2O(g)的生成速率增大
D.保持压强不变,充入氖气,H2O(g)、H2(g)的生成速率减小
 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
【题目】已知![]() (x)、
(x)、![]() (y)、
(y)、![]() (z) 互为同分异构体,下列说法不正确的是( )
(z) 互为同分异构体,下列说法不正确的是( )
A. Z的二氯代物只有三种
B. x、y、z中只有x的所有原子可能处于同一平面
C. x的同分异构体只有y和z两种
D. x、y可使溴的四氯化碳溶液因发生加成反应而褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置能达到实验目的是(夹持仪器未画出)( )
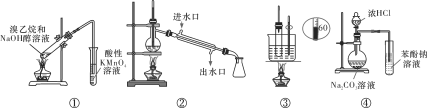
A. 装置①用于检验溴乙烷消去生成的乙烯 B. 装置②用于石油的分馏
C. 装置③用于实验室制硝基苯 D. 装置④可证明酸性:盐酸>碳酸>苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I(C11H12O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基,I可以用E和H在一定条件下合成:
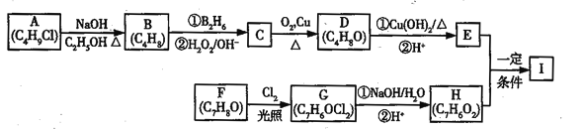
已知以下信息:
①A的核磁共振氢谱表明其只有一种化学环境的氢;
②R﹣CH=CH2![]() R﹣CH2CH2OH;
R﹣CH2CH2OH;
③化合物F苯环上的一氯代物只有两种;
④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
回答下列问题:
(1)A的化学名称为_______________________________;
(2)D的结构简式为_______________________________;
(3)E中的官能团名称为___________________________;
(4)F生成G的化学方程式为__________________________,该反应类型为______________;
(5)I的结构简式为_________________________________。
(6)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:①苯环上只有两个取代基,②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2,共有____种(不考虑立体异构)。J的一个同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂均过量):
称取粗盐![]()
![]()
![]()
![]()
![]() 滤液
滤液![]()
![]() 精盐。
精盐。
下列叙述正确的是
A.第④发生的反应只有CaCl2+Na2CO3=CaCO3↓+2NaCl
B.③中的试剂可以是NaOH溶液也可以是KOH溶液
C.步骤②和④顺序可以颠倒
D.⑤步操作用到的玻璃仪器只有烧杯、漏斗和玻璃棒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积固定的密闭容器中发生反应:![]() 。下列叙述中不能说明上述反应已达到化学平衡状态的是
。下列叙述中不能说明上述反应已达到化学平衡状态的是
A.混合气体的密度不变
B.体系的压强不变
C.混合气体的平均相对分子质量不变
D.反应体系中乙醇的物质的量浓度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表是学习物质结构和性质的重要工具,下面是元素周期表的一部分,表中所列字母A、D、E、G、Q、M、R分别代表某一化学元素。请用所给元素回答下列问题。
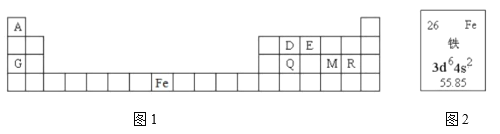
(1)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为_____________。R原子的最外层电子排布式____________________________;原子核外有________种能量不同的电子。R原子最外层有________种运动状态不同的电子。
(2)元素Fe在元素周期表中的位置是__________________________________________。图2中,55.85表示__________________________________________________________。
(3)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是____________________(填离子符号)。
(4)M、D两种元素形成的化合物含有的化学键类型是____________________(填“极性键”或“非极性键”),其分子是____________________(填“极性分子”或“非极性分子”)。D、Q的最高价氧化物形成的晶体相比,熔点较高的是____________________(用化学式表示)。
(5)表中金属性最强的元素与铝元素相比较,可作为判断金属性强弱依据的是________(选填编号)。
a.能否置换出铝盐溶液中铝
b.![]() 能否溶解在该元素最高价氧化物对应水化物中
能否溶解在该元素最高价氧化物对应水化物中
c.单质与氢气化合的难易程度
d.单质与同浓度的稀盐酸发生反应的剧烈程度
(6)在![]() 溶液中逐滴加入G的最高价氧化物的水化物,现象是先产生白色沉淀,然后白色沉淀逐渐消失。请用以上某化学方程式证明Al与G金属性的强弱。______________________。O的非金属性比N强,请用元素周期律的知识分析原因。___________________。
溶液中逐滴加入G的最高价氧化物的水化物,现象是先产生白色沉淀,然后白色沉淀逐渐消失。请用以上某化学方程式证明Al与G金属性的强弱。______________________。O的非金属性比N强,请用元素周期律的知识分析原因。___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
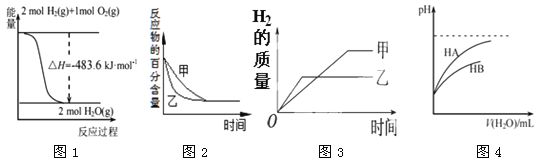
A.图1表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8 kJ·mol-1
B.图2表示压强对可逆反应2A(g)+2 B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
C.图3表示等质量的钾、钠分别与足量水反应,则甲为钠
D.图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同条件下NaA溶液的pH大于同浓度的NaB溶液的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铵明矾![]() 常用作食品工业的膨松剂、某化学兴趣小组设计如下实验方案制备铵明矾并测定其组成。
常用作食品工业的膨松剂、某化学兴趣小组设计如下实验方案制备铵明矾并测定其组成。
已知:
①铵明矾为无色透明晶体,在水中的溶解度随温度升高而增大。
②铵明矾在250℃时失去结晶水,280℃时开始分解。
I.制备铵明矾
甲同学制备铵明矾的简易流程如图所示。
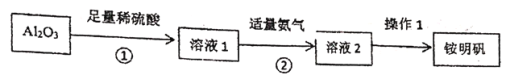
(1)步骤②中发生反应的离子方程式为____。
(2)操作1为____、___、过滤、洗涤、干燥。
II.测定铵明矾的组成
(3)乙同学设计下列实验装置测定铵明矾中结晶水的含量(装置B和装置C中的碳石灰均足量)。
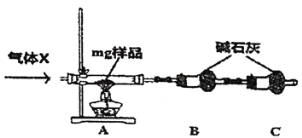
①装置A中应控制反应温度的范围为___﹔气体x不能选用___(填“N2”“Ne”或“CO2”)。
②装置C的作用为___。
(4)丙同学利用下列实验装置测定铵明矾中氮元素的含量。
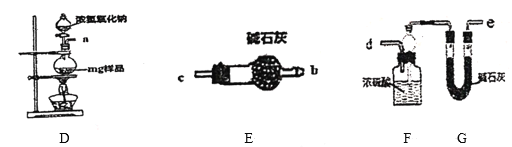
①按照气流从左到右的方向,上述装置的连接顺序为___(填装置接口处的小写字母)。
②用该装置进行实验时,即使氢氧化钠足量且实验过程中无NH3逸出,测得样品中氮元素的含量仍偏低,其原因可能是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com