
| A. | 由被氧化的元素组成的反应物是氧化剂 | |
| B. | 在一个氧化还原反应中,氧化反应和还原反应同时发生 | |
| C. | 由化合态转变为游离态的变化一定是还原反应 | |
| D. | 氧化还原反应的实质是元素化合价的升降 |
分析 A、还原剂被氧化;
B、氧化还原反应中氧化反应和还原反应同时发生;
C、某元素由化合态变成游离态,可能失去电子也可能得到电子,则在反应中可能被氧化也可能被还原;
D、氧化还原反应的特征为化合价的升降.
解答 解:A.被氧化的物质在反应中失去电子,是还原剂,故A错误;
B、氧化还原反应中有失电子,必有得电子,所以在氧化还原反应中氧化反应和还原反应同时发生,故B正确;
C、某元素由化合态变成游离态,在反应中可能被氧化也可能被还原,如反应H2S+SO2═3S↓+2H2O中,S元素既被氧化又被还原,故C错误;
D、氧化还原反应的特征为化合价的升降,其实质为电子的转移,故D错误;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握氧化还原反应中的基本概念及常见的实例为解答的关键,注意利用实例分析选项,题目难度不大.


科目:高中化学 来源: 题型:解答题
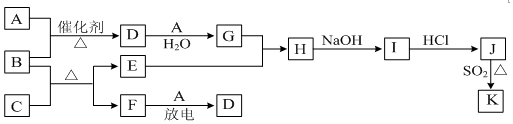
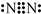
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
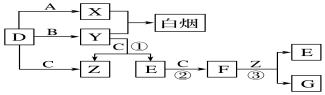
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 如图是我校化学实验室浓盐酸试剂标签上的部分内容.
如图是我校化学实验室浓盐酸试剂标签上的部分内容.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO42- | B. | SO32- | C. | S | D. | S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
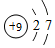 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol A+2mol B+1mol C | |
| B. | 0.6mol C+0.6mol D+0.2mol B+0.3mol A | |
| C. | 0.6mol A+0.2mol D+0.1mol C | |
| D. | 0.25mol A+0.5mol B+0.1mol C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{23}^{51}$V和${\;}_{23}^{50}$V互为同位素 | |
| B. | ${\;}_{23}^{51}$和${\;}_{23}^{50}$V的质量数相同 | |
| C. | ${\;}_{23}^{51}$V和${\;}_{23}^{50}$V是同一种核素 | |
| D. | ${\;}_{23}^{51}$V和${\;}_{23}^{50}$V的核外电子数与中子数均为23 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
在一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应A(g)+2B(g) C(g)+D(g)已达到平衡状态的是( )
C(g)+D(g)已达到平衡状态的是( )
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④混合气体的总物质的量 ⑤混合气体的平均相对分子质量 ⑥v(C)与v(D)的比值 ⑦混合气体的总质量
A.②③④⑤⑥⑦ B.①③④⑤ C.①②③④⑤⑦ D.①③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com