
| ѡ�� | ʵ����������� | ʵ����� |
| A | �����ݵ�������Һ�зֱ�μ�NaCl��Һ�� CuSO4��Һ�����й������� | �����ʾ������˱��� |
| B | ȡ����Fe��NO3��2������ˮ�ܽ⣬��ϡ�����ữ�� �μ�KSCN��Һ����Һ��Ϊ��ɫ | ��Fe��NO3��2�����Ѿ� ���� |
| C | ������ij���ʵ���Һ�μӵ����Ƶ�������Һ�У� ˮԡ���Ⱥ����������� | ������һ������ȩ�� |
| D | ͬ�����£��ֱ�0.1mol?L-1������ʹ���� �е�����ʵ�飬����ᴮ���ĵ��ݽϰ� | ���������� |
| A��A | B��B | C��C | D��D |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| (1)B2H4 |
| (2)H2O/OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A���ȿ����ܴ��������������ӷ������� |
| B��SO2������ķ�Ӧ����ʽ��SO2+2H2O+Br2��H2SO4+2HBr |
| C��������ѭ�����õ�������SO2��Br2��Cl2�ȶ��� |
| D��û�в���ֱ�������庣ˮ�õ����������Ҫԭ����Ϊ�˽��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1.09g |
| B��1.20 g |
| C��1.36g |
| D��1.63g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| CO2��mol�� | 0.05 | 0.15 | 0.6 |
| NaX��mol�� | |||
| Na2CO3��mol�� | |||
| NaHCO3��mol�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����Թܼд��Թܵ��������ϼ�ס����ܿ�Լ����֮һ�����ֳ��Թܼг���ĩ�ˣ����м��� |
| B���Ʊ���������ʱ�����Ҵ����������μ��뵽Ũ������ |
| C���Ѳ����ܲ���������ʱ���ú��֣�������ˮʪ��IJ����ܲ���ˣ��������������� |
| D��ʵ��ʱ���������¶ȼ�ˮ�����õιܽ�ˮ����������ˮ���Сƿ�У����Ƶ��¶ȼƲ���װ����۵Ĺ��ƿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2 | B��3 | C��4 | D��5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� ����ʳ��ˮ |
B�� ȡ�����ĩ |
C�� ����Һ�� |
D�� �㵹Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
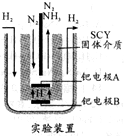 ����һ����Ҫ�Ļ���ԭ�ϣ����ĺϳɺ�Ӧ���ǵ�ǰ����Ҫ�о�����֮һ��
����һ����Ҫ�Ļ���ԭ�ϣ����ĺϳɺ�Ӧ���ǵ�ǰ����Ҫ�о�����֮һ��| 1 |
| 2 |
| ʱ��/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c��NH3��/��mol��L-l�� | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com