
【题目】铝元素含量居金属首位,主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。铝的单质及其化合物在生产、生活、科研等领城应用广泛。
Ⅰ.工业上用铝土矿制备铝的某种化合物的工艺流程如图:

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①该过程中涉及某氧化还原反应如下,请完成:___Fe2++___ClO-+___=___Fe(OH)3↓+___C1-+___
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为___(选填代号)
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
③由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、___(填操作名称)、过滤、洗涤。
Ⅱ.铵明矾(NH4Al(SO4)212H2O)是常见的食品添加剂,在日常生活、生产中也占有一席之地。
(1)铵明矾可用于净水,用离子方程式表示其净水原理___;向其溶液中逐滴加入NaOH溶液至过量,可观察到的现象是___。
(2)实验证明铵明矾高温分解后气体的组成成份是NH3、N2、SO3、SO2和H2O,且相同条件下测得生成N2和SO2的体积比是定值,V(N2):V(SO2)=___。
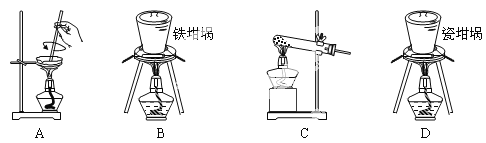
(3)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为___(填代号)。
【答案】2 1 5H2O 2 1 4H+ C 冷却结晶,过滤 铵明矾溶液电离出的铝离子水解得到氢氧化铝胶体,可以吸附悬浮物质,可以用于净水 先产生白色沉淀,后产生有刺激性气味的气体,再加入过量的NaOH溶液,白色沉淀逐渐溶解并消失 1:3 B
【解析】
Ⅰ.图示工艺流程为:铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)加入稀盐酸,得到滤渣为二氧化硫,滤液中含有铁离子、亚铁离子和氯离子;加入漂白液后亚铁离子氧化成铁离子,铁离子水解生成氢氧化铁沉淀;滤液B为氯化铝溶液;二氧化硫与氢氧化钠在铁坩埚中焙烧生成硅酸钠,
(1)①依据流程分析,滤液中含有氯化铁、氯化亚铁、氯化铝,在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性,次氯酸根离子具有氧化性氧化亚铁离子为铁离子在溶液中形成氢氧化铁沉淀除去;依据氧化还原反应电子守恒和原子守恒配平计算写出;
②滤液B中铝元素为氯化铝,依据氢氧化铝溶液强酸强碱,不溶于弱碱选择;
加入浓盐酸抑制氯化铝的水解,蒸发浓缩冷却结晶,过滤洗涤;
Ⅱ.(1)铵明矾溶液中铝离子水解,溶液呈酸性,得到氢氧化铝胶体,可以用于净水;向溶液中加入氢氧化钠溶液,首先与溶液中铝离子反应生成氢氧化铝沉淀,再与氨气根离子反应生成氨气,再加入过量的NaOH溶液溶解氢氧化铝;
(2)根据电子转移守恒确定n(N2):n(SO2),相同条件下气体体积之比等于其物质的量之比.
(3)A.蒸发皿中含有二氧化硅和氢氧化钠反应;
B.铁坩埚可以熔融二氧化硅和氢氧化钠;
C.玻璃中含二氧化硅和氢氧化钠反应;
D.瓷坩埚含有二氧化硅和氢氧化钠反应。
Ⅰ. (1)①滤液中含有氯化铁、氯化亚铁、氯化铝,在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性,次氯酸根离子具有氧化性,氧化亚铁离子为铁离子,在溶液中形成氢氧化铁沉淀除去;次氯酸根离子被还原为氯离子,反应的离子方程式为2Fe2++ClO+5H2O=2Fe(OH)3↓+C1+4H+;
故答案为:2;1;5H2O;2;1;4H+;
②滤液中含有的是氯化铝溶液,将滤液B中的铝元素以沉淀形式析出,
A.氢氧化钠溶液可以沉淀铝离子但过了会溶解氢氧化铝,氢氧化钠不是最佳试剂,故A错误;
B.硫酸溶液不与铝离子反应,故B错误;
C.氨水是弱碱不能溶解氢氧化铝,过量的氨水和铝离子形成氢氧化铝沉淀过滤得到氢氧化铝固体,故C正确;
D.二氧化碳和氯化铝不反应,无法生成氢氧化铝沉淀,故D错误;
故答案为:C;
③加入浓盐酸抑制氯化铝的水解,蒸发浓缩,冷却结晶,过滤,洗涤,
故答案为:冷却结晶,过滤;
Ⅱ. (1)铵明矾溶液中铝离子水解得到氢氧化铝胶体,可以吸附悬浮物质,可以用于净水;向溶液中加入氢氧化钠溶液,首先与溶液中铝离子反应生成氢氧化铝沉淀,再与氨气根离子反应生成氨气,再加入过量的NaOH溶液溶解氢氧化铝,现象为:先产生白色沉淀,后产生有刺激性气味的气体,再加入过量的NaOH溶液,白色沉淀逐渐溶解并消失,
故答案为:铵明矾溶液电离出的铝离子水解生成氢氧化铝胶体,有吸附作用,故铵明矾能净水;先产生白色沉淀,后产生有刺激性气味的气体,再加入过量的NaOH溶液,白色沉淀逐渐溶解并消失;
(2)根据电子转移守恒:2×[0(3)]×n(N2)=n(SO2)×(64),故n(N2):n(SO2)=1:3,相同条件下气体体积之比等于其物质的量之比,故V(N2):V(SO2)=1:3,
故答案为:1:3.
(3)A.蒸发皿中含有二氧化硅和氢氧化钠反应,不能用于SiO2和NaOH焙烧制备硅酸钠,故A错误;
B. 铁坩埚可以熔融二氧化硅和氢氧化钠,可在铁坩埚中用SiO2和NaOH焙烧制备硅酸钠,故B正确;
C. 玻璃中含二氧化硅和氢氧化钠反应,不能用于SiO2和NaOH焙烧制备硅酸钠,故C错误;
D. 瓷坩埚含有二氧化硅和氢氧化钠反应,不能用于SiO2和NaOH焙烧制备硅酸钠,故D错误;
故答案为:B。


科目:高中化学 来源: 题型:
【题目】下列表述正确的是( )
A.工夫茶主要程序有治壶、投茶、出浴、淋壶、烫杯、酾茶、品茶等其中涉及的操作方法有:溶解、萃取、过滤、蒸馏
B.含棉、麻、丝、毛及合成纤维的废旧衣物燃烧处理时都只生成![]() 和
和![]()
C.工业上生产玻璃、水泥、漂白粉及用铁矿石冶炼铁,均需要用石灰石为原料
D.港珠澳大桥设计使用寿命120年,水下钢柱镶铝块防腐的方法为牺牲阴极保护法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器内,800 ℃时,0.02molNO(g)和0.01molO2(g)反应生成NO2(g)的体系中,n(NO)随时间的变化如下表所示:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应_____(填“是”或“不是”)可逆反应,在第5 s时,NO的转化率为_______。
(2)如图中表示NO2变化曲线的是________,用O2表示从0~2 s内该反应的平均速率v=________。
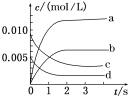
(3)能说明该反应已达到平衡状态的是________。
a v(NO2)=2v(O2) b 容器内压强保持不变
c v逆(NO)=2v正(O2) d 容器内密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
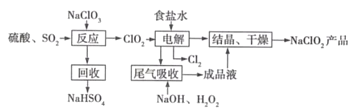
回答下列问题:
(1)NaClO2中Cl的化合价为_______。
(2)写出“反应”步骤中生成ClO2的化学方程式_______。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为________、________。“电解”中阴极反应的主要产物是______。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2。此吸收反应中,氧化剂与还原剂的物质的量之比为________,该反应中氧化产物是_________。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为____。(计算结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在200℃时,将amol H2(g)和bmol I2(g)充入到体积为V L的密闭容器中,发生反应:I2(g)+H2(g)![]() 2HI(g)。
2HI(g)。
(1)反应刚开始时,由于c(H2)= ______,c(I2)= ______,而c(HI)=______,所以化学反应速率V正最大,而V逆最小(为零)。
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为c(H2)______,c(I2)______,而c(HI)______,从而化学反应速率v(正)______,而v(逆)______。
(3)当反应进行到v(正)与v(逆)相等时,此可逆反应就达到了平衡。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸在食品、医药等方面有着广泛用途。一种合成阿魏酸的反应可表示为:
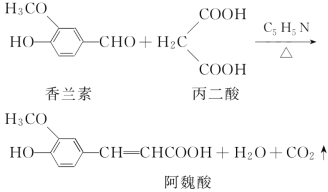
则下列说法不正确的是( )
A.丙二酸与乙二酸互为同系物
B.由题中信息可知阿魏酸甲酯的分子式为C11H12O4
C.香兰素、阿魏酸都是芳香族化合物
D.可用溴水检测上述反应中香兰素是否完全转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是![]()
A.反应![]() 室温下不能自发进行,则该反应的
室温下不能自发进行,则该反应的![]()
B.配制硫酸亚铁溶液时,需将![]() 先溶于硝酸再用蒸馏水稀释,最后加少量铁粉
先溶于硝酸再用蒸馏水稀释,最后加少量铁粉
C.![]() 溶液加蒸馏水稀释,
溶液加蒸馏水稀释,![]() 的水解程度增大,溶液的pH减小
的水解程度增大,溶液的pH减小
D.在硫酸钡悬浊液中加入足量饱和![]() 溶液处理,向所得沉淀中加入盐酸有气体产生,说明
溶液处理,向所得沉淀中加入盐酸有气体产生,说明![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H是一种香料,可用如图的设计方案合成。

已知:①在一定条件下,有机物有下列转化关系:
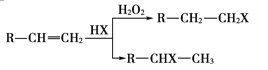 (X为卤素原子)
(X为卤素原子)
②烃A和等物质的量的HCl在不同的条件下发生加成反应,既可以生成只含有一个甲基的B,也可以生成含有两个甲基的F。
(1)D的结构简式为__。
(2)写出D与银氨溶液反应的化学反应方程式___。
(3)A→B和F→G的化学反应类型为___。
(4)E+G→H的化学反应方程式是___。
(5)H有多种同分异构体,其中含有一个羧基,且其烃基上一氯代物有两种的是___(用结构简式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质间有如下转化关系,请按要求填空。
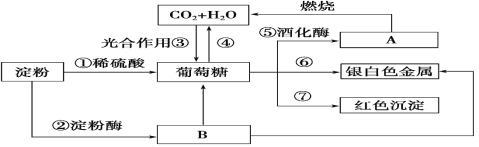
(1)在制镜工业和热水瓶胆镀银时,常利用上述反应________(填序号)。
(2)反应①②的反应类型为_______(填选项字母)。
A.氧化反应 B.加成反应 C.水解反应 D.消去反应
(3)反应⑦可用于检验糖尿病病人尿液中的含糖量,该反应的化学方程式为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com