
ij����Cr2O72����ˮ����������泥�FeSO4��(NH4)2 SO4��6H2O�ݴ�������Ӧ����Ԫ�غ�Ԫ����ȫת��Ϊ�������ó��������õ�n molFeO��FeyCrxO3������Cr�Ļ��ϼ�Ϊ+3�ۡ������Ǵ��������е�ʵ����ģ����������������
| A��������������淋����ʵ���Ϊn(2-x)mol |
B��������ˮ��Cr2O72�� �����ʵ���Ϊ mol mol |
| C����Ӧ��ת�Ƶĵ���Ϊ3nx mol |
| D����FeO��FeyCrxO3��3x=y |
A
�������������A��������Ԫ���غ�ã�������������淋����ʵ���Ϊn��y+1��mol,����B�����ݸ�Ԫ���غ㣬�����и�Ԫ�ص����ʵ���Ϊnx,���Դ�����ˮ��Cr2O72�� �����ʵ���Ϊ mol����ȷ��C����ˮ��Cr2O72���Ļ��ϼ�Ϊ+6�ۣ���Ӧ��Ϊ+3�ۣ����Է�Ӧ��ת�Ƶĵ���Ϊ3��2��
mol����ȷ��C����ˮ��Cr2O72���Ļ��ϼ�Ϊ+6�ۣ���Ӧ��Ϊ+3�ۣ����Է�Ӧ��ת�Ƶĵ���Ϊ3��2�� mol ="3nx" mol����ȷ��D����Ӧ�и��õ�����Ϊ3nx mol����������ת��Ϊ������ʧȥnymol���ӣ����ݵ�ʧ�����غ㣬��3nx=ny����������3x=y����ȷ����ѡA��
mol ="3nx" mol����ȷ��D����Ӧ�и��õ�����Ϊ3nx mol����������ת��Ϊ������ʧȥnymol���ӣ����ݵ�ʧ�����غ㣬��3nx=ny����������3x=y����ȷ����ѡA��
���㣺����������ԭ��Ӧ��Ԫ���غ㡢��ʧ�����غ��Ӧ��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��27��2gCu��Cu2O�Ļ�����м���ijŨ�ȵ�ϡ����0��5L������������ȫ��Ӧ������NO ��Cu(NO3)2����������Һ�м���1��0mol/L ��NaOH��Һ1��0L����ʱ��Һ�����ԣ�������������ȫ��������������Ϊ39��2g�������й�˵������ȷ����
| A��Cu��Cu2O �����ʵ���֮��Ϊ2:1 |
| B����������ʵ���Ũ��Ϊ2��6mol/L |
| C��������NO�ڱ�״���µ����Ϊ4��48L |
| D��Cu��Cu2O�����ᷴӦ��ʣ��HNO3Ϊ0��2mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
4.6gͭþ�Ͻ���ȫ�ܽ���100ml�ܶ�Ϊ1.40g/ml����������Ϊ63%��Ũ�����У��õ�4480mlNO2��336 ml N2O4�Ļ������(��״��)����Ӧ�����Һ�м���1.0mol/LNaOH��Һ������ǡ��ȫ������ʱ������˵������ȷ���� �� ��
| A���úϽ���ͭ��þ�����ʵ���֮����46:69 |
| B����Ũ������HNO3�����ʵ���Ũ����14.0mol/L |
| C����������8.51 g |
| D������ǡ����ȫ����ʱ������NaOH��Һ�������230mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����Ǻ�ˮ�ۺ�Ӧ������ȡþ����ķ�Ӧ������������ԭ��Ӧ����
| A����±�м���ʯ����MgCl2+ Ca(OH)2 = CaCl2 +Mg(OH)2 |
| B����±��ͨ������2Br- + Cl2 = 2Cl- + Br2 |
C���ȼҵ���ʳ��ˮ2NaCl + 2H2O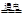 2NaOH + H2��+ Cl2�� 2NaOH + H2��+ Cl2�� |
D������Ȼ�þMgCl2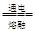 Mg + Cl2�� Mg + Cl2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ�ྻ������ձ��м���44.4gAl����Fe�ۻ���Ȼ�������������ᣬ�������������26.88L�������û�������500mL14 mol��L-1��HNO3�У������Ƿ����ۻ��������������壨��״���²ⶨ����ͼ��ʾ������HNO3�Ļ�ԭ����ΪNO��NO2����ô�����ϴ���һʱ�̿�ʼ����NO����?������Ũ��С��9mol/LΪϡHNO3��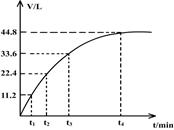
| A��t1 | B��t2 | C��t3 | D��t4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
Na2FeO4��һ�ָ�Ч���ˮ��������һ���Ʊ�Na2FeO4�ķ������û�ѧ����ʽ��ʾ���£�2FeSO4��6Na2O2=2Na2FeO4��2Na2O��2Na2SO4��O2��������˵���в���ȷ����( )
| A��Na2O2��������Ӧ��ֻ�������� |
| B��Na2FeO4���������������ǻ�ԭ���� |
| C��Na2FeO4����ˮʱ������ɱ���������ڴ���ˮʱ�������徻ˮ |
| D��2 mol FeSO4������Ӧʱ������10 mol���ӷ���ת�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ȡm gþ���Ͻ���һ��Ũ�ȵ�ϡ������ǡ����ȫ�ܽ�(����Ļ�ԭ����ֻ��NO)����Ӧ��Ļ����Һ�еμ�b mol��L��1 NaOH��Һ�����μӵ�V mLʱ���õ���������ǡ��Ϊ���ֵn g���������йظ�ʵ���˵������ȷ����(����)��
�ٳ�����OH��������Ϊ(n��m)g
��ǡ���ܽ����Һ�е�NO�����ʵ���Ϊ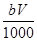 mol
mol
�۷�Ӧ������ת�Ƶĵ�����Ϊ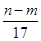 mol
mol
�ܱ�״��������NO�����Ϊ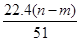 L
L
����Ͻ�Ӧ����������ʵ���Ϊ(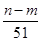 ��
��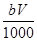 )mol
)mol
| A��5�� | B��4�� | C��3�� | D��2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��18 gͭ�����Ļ����Ͷ��200 mLϡ�����У���ַ�Ӧ��õ���״����2.24 L NO��ʣ��9.6 g��������������200 mL��Ũ�ȵ�ϡ���ᣬ������ȫ�ܽ⣬�ֵõ���״����2.24 L NO������Ӧ�����Һ�м���KSCN��Һ����Һ����죬������˵����ȷ����(����)
| A��ԭ�������ͭ������0.15 mol |
| B��ϡ��������ʵ���Ũ��Ϊ1 mol/L |
| C����һ��ʣ���9.6 g����Ϊͭ���� |
| D���ټ�������200 mLϡ���ᣬ�ֵõ���״����2.24 L NO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��Cu2S+2Cu2O 6Cu+SO2����Ӧ��,����˵������ȷ����(����)
6Cu+SO2����Ӧ��,����˵������ȷ����(����)
| A��Cu2O�ڷ�Ӧ�б����� |
| B��Cu2S�ڷ�Ӧ�м������������ǻ�ԭ�� |
| C��Cu���������������ǻ�ԭ���� |
| D������Ӧ��ת��12 mol����,������6 mol Cu |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com