
下列说法中错误的是 ( )
A.化学反应中的能量变化通常表现为热量的变化
B.化学键的断裂和形成是化学反应中能量变化的主要原因
C.需要加热才能发生的反应一定是吸热反应
D.反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量
科目:高中化学 来源: 题型:
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的是 ( )
A.X、Y、Z、W的原子半径依次减小
B.W与X形成的化合物中只含离子键
C.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点
D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物由C、H、O三种元素组成,它的红外吸收光谱表明有羟基O—H键和烃基上
C—H键的红外吸收光峰,且烃基与羟基上氢原子个数之比为2:1,该有机物可能为
A. 乙二醇 B. 乙醇 C. 甲醇 D. 丙三醇
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:
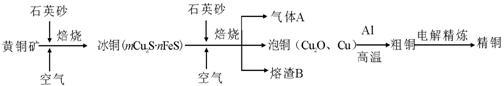
(1)气体A中的大气污染物可选用下列试剂中的 吸收。
A.浓H2SO4 B.稀HNO3 C.NaOH溶液 D.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在 (填离子符号),检验溶液中还存在Fe2+的方法是 (注明试剂.现象)。
(3)由泡铜冶炼粗铜的化学反应方程式为 。
(4)以CuSO4溶液为电解质溶液进行粗铜(含Al.Zn.Ag.Pt.Au等杂质)的电解精炼,下列说法正确的是
A.电能全部转化为化学能 B.粗铜接电源正极,发生氧化反应
C.溶液中Cu 理 _______________________________________________________________________2+向阳极移动 D.利用阳极泥可回收Ag、Pt、Au等金属
(5)利用反应可制备CuSO4,若将该反应2Cu2+ + O2 + 2H2SO4 = 2CuSO4 + 2H2O设计
为原电池,其正极电极反应式为
查看答案和解析>>
科目:高中化学 来源: 题型:
物质A ~ G有下图所示转化关系(部分反应物、生成物
未列出)。其中A为某金属矿的主要成分,经过一系列反应可
得到气体B和固体C。单质C可与E的浓溶液发生反应,G为砖红色沉淀。
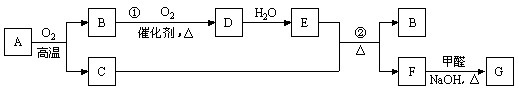
请回答下列问题:
(1)写出下列物质的化学式:B___________、G___________。
(2)反应②的化学方程式是__________________________________________________。
(3)利用电解可提纯C物质,现以碱性锌锰电池为外电源,在该电解反应中电解质溶液是_______________,阳极物质是______________。MnO2是碱性锌锰电池的正极材料,电池放电时,正极的电极反应式为_____________________________________________。
(4)将0.20 mol B和0.10 mol O2充入一个固定容积为5 L的密闭容器中,在一定温度并有催化剂存在下,进行反应①,经半分钟后达到平衡,测得容器中含D 0.18 mol,则v(O2)== ______________mol/(L·min);若温度不变,继续通入0.20 mol B和0.10 mol O2,则平衡________________移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,________mol < n(D) < ________mol。
 (5)写出F G转化过程中,甲醛参与反应的化学方程式:
(5)写出F G转化过程中,甲醛参与反应的化学方程式:
___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是 ( )
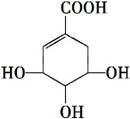
莽草酸
A.分子式为C7H6O5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.在水溶液中羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机物的说法中,不正确的是 ( )
A.淀粉、油脂、蛋白质在一定条件下都能发生水解反应
B.“乙醇汽油”是在汽油里加入适量乙醇而成的一种燃料,它是一种新型化合物
C.除去乙酸乙酯中残留的乙酸、乙醇,可加过量饱和Na2CO3溶液振荡后,静置分液
D.淀粉遇碘酒变蓝色,葡萄糖能与新制Cu(OH)2发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
铁、铜单质及其化合物应用范围很广。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按如图步骤进行提纯:
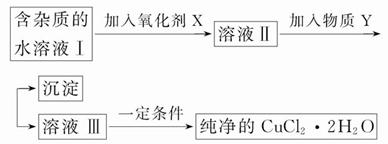
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9.0 | 6.7 |
请回答下列问题:
(1)加入氧化剂的目的是 。
(2)最适合作氧化剂X的是 。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(3)加入的物质Y是 。
(4)若不用物质Y而是直接用碱能不能达到目的? (填“能”或“不能”)。若能,不用回答;若不能,试解释原因 。
(5)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体? (填“能”或“不能”)。若能,不用回答;若不能,回答该如何操作?
。
(6)若向溶液Ⅱ中加入碳酸钙,产生的现象是
。
查看答案和解析>>
科目:高中化学 来源: 题型:
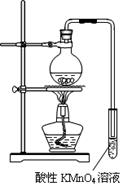 某学习小组探究溴乙烷的消去反应并验证产物。
某学习小组探究溴乙烷的消去反应并验证产物。
实验原理:CH3CH2Br + NaOH 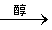 CH2=CH2↑ + NaBr + H2O
CH2=CH2↑ + NaBr + H2O
实验过程:组装如图所示装置,检查装置气密性,向烧瓶中注入10mL溴乙烷和15mL饱和氢氧化钠乙醇溶液,微热,观察实验现象。一段时间后,观察到酸性KMnO4溶液颜色褪去。
(1)甲同学认为酸性KMnO4溶液颜色褪去说明溴乙烷发生了消去反应,生成了乙烯;而乙同学却认为甲同学的说法不严谨,请说明原因: 。
(2)丙同学认为只要对实验装置进行适当改进,就可避免对乙烯气体检验的干扰,改进方法为: 。
改进实验装置后,再次进行实验,却又发现小试管中溶液颜色褪色不明显。该小组再次查阅资料,对实验进行进一步的改进。
资料一:溴乙烷于55℃时,在饱和氢氧化钠的乙醇溶液中发生取代反应的产物的百分比为99%,而消去反应产物仅为1%。
资料二:溴乙烷发生消去反应比较适宜的反应温度为90℃~110℃,在该范围,温度越高,产生乙烯的速率越快。
资料三:溴乙烷的沸点:38.2℃。
(3)结合资料一、二可知,丙同学改进实验装置后,溶液颜色褪色不明显的原因可能是 ,此时发生反应的化学方程式为: 。
(4)结合资料二、三,有同学认为应将实验装置中烧瓶改成三颈烧瓶并增加两种仪器,
这两种仪器是① 。 ② 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com