
 ��1����ӦA+3B?2C+2D�����ֲ�ͬ����µķ�Ӧ���ʷֱ����£�
��1����ӦA+3B?2C+2D�����ֲ�ͬ����µķ�Ӧ���ʷֱ����£����� ��1����������֮�ȵ��ڻ�ѧ������֮�ȣ��ʲ�ͬ�����ʱ�ʾ�ķ�Ӧ�������仯ѧ�������ı�ֵԽ�����ʾ�ķ�Ӧ����Խ�죻
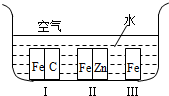
��2�����γ�ԭ��أ�I��FeΪ����������ʴ������FeΪ������ZnΪ������Fe�����������з�����ѧ��ʴ���绯ѧ��ʴ�����ʴ��ڻ�ѧ��ʴ�����ʣ�
��� �⣺��1����������֮�ȵ��ڻ�ѧ������֮�ȣ��ʲ�ͬ�����ʱ�ʾ�ķ�Ӧ�������仯ѧ�������ı�ֵԽ�����ʾ�ķ�Ӧ����Խ�죺
��v��B��=3.6mol•L-1•min-1=0.06mol•L-1•s-1��$\frac{v��B��}{3}$=0.02mol•L-1•s-1��
��$\frac{v��A��}{1}$=0.15mol•L-1•s-1��
��$\frac{v��C��}{2}$=0.25mol•L-1•s-1��
��$\frac{v��D��}{2}$=0.3mol•L-1•s-1��
�ʷ�Ӧ���ʢܣ��ۣ��ڣ��٣�
�ʴ�Ϊ���ܣ��ۣ��ڣ��٣�
��2�����γ�ԭ��أ�I��FeΪ����������ʴ������FeΪ������ZnΪ������Fe�����������з�����ѧ��ʴ��������ʴ����˳���ǣ���
�ʴ�Ϊ����
���� ���⿼�鷴Ӧ���ʿ����Ƚϡ�������ʴ��������ѶȲ��ȽϷ�Ӧ���ʳ��õ����ַ�������1����һ������ͬһ��Ӧ�еIJ�ͬ���ʵķ�Ӧ����ת����ͬһ���ʵķ�Ӧ���ʣ��ٽ�С�Ƚϣ���2����ֵ�����ø����ʵ�����ʾ�ķ�Ӧ���ʳ��Զ�Ӧ�����ʵĻ�ѧ����������ֵ��ķ�Ӧ���ʿ죮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 12lg CCl2F2��������ԭ����Ϊ2NA | |
| B�� | ���³�ѹ��l mol NO2������ˮ��Ӧ����NA��NO3һ���� | |
| C�� | �Ȼ��������Ħ����������NA����ԭ�Ӻ�NA����ԭ�ӵ�����֮�� | |
| D�� | 124g Na2O����ˮ��������Һ�к���O2-������Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


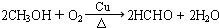 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
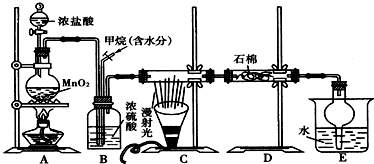
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ƹ��� | B�� | Ũ���� | C�� | Ũ���� | D�� | ��ʯ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ǿ����Һ�д���������Fe��OH��3��Ӧ����Na2FeO4��3ClO-+2Fe��OH��3=2 FeO42-+3Cl-+H2O+4H+ | |
| B�� | ̼�������Һ����������������Һ��Ӧ��NH4++OH-=NH3•H2O | |
| C�� | NaHSO4��Һ�е���Ba��OH��2��Һ�����ԣ�H++SO42-+Ba2+ʮOH-�TBaSO4��+H2O | |
| D�� | ������̼��������Һ���뵽����������Һ�У�HCO3-+Ba2++OH-=BaCO3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Oԭ�Ӳ�ȡsp2�ӻ� | B�� | Oԭ�Ӳ�ȡsp�ӻ� | ||
| C�� | �����д�����λ�� | D�� | �����д��ڷǼ��Լ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
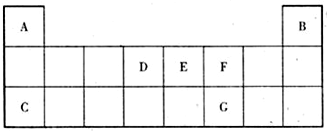
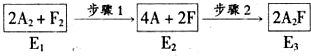
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com