
【题目】某实验的实验装置如图所示,回答下列有关该实验的问题。
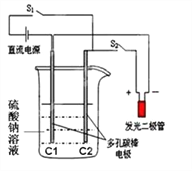
(1)该实验所用的石墨棒须经过预处理;先经高温火焰灼烧到红热,再迅速浸入冷 水中。这种预处理的目的是:_____。
(2)要使发光二极管发亮,实验时的操作顺序是:先关闭 S1,打开 S2,电解一段时 间后,再打开 S1,关闭 S2 ,请写出整个实验过程中的能 量转化形式_____
(3)写出下列操作时的电极反应式,并注明电极名称:
① 按下开关 S1:C1 附近发生 2H2O+2e— =H2↑+2OH— 的电极反应
② 断开开关 S1,迅速按下开关 S2:(提示:此时 C1 附近溶液显碱性,C2 附近溶液显酸性)
C2 _____,_____
【答案】 使石墨棒表面变得粗糙,有利于吸附气体 电能→化学能→电能(或电能→化学能→电能→光能) 正极 O2+ 4H++ 4e― = 2H2O
【解析】试题分析:经高温火焰灼烧到红热,再迅速浸入冷水中,可以使石墨棒表面变得粗糙;关闭 S1,打开 S2,构成电解池,C1是阴极、C2是阳极,电解硫酸钠溶液,实质是电解水,阴极生成氢气、阳极生成氧气;打开S1,关闭 S2时,构成氢氧燃料电池;
解析:(1)经高温火焰灼烧到红热,再迅速浸入冷水中,可以使石墨棒表面变得粗糙,有利于吸附气体;(2)根据以上分析,关闭 S1,打开 S2,构成电解池,电能转化为化学能;打开S1,关闭 S2时,构成氢氧燃料电池,化学能转化为电能;所以整个实验过程中的能量转化形式电能→化学能→电能;断开开关 S1,迅速按下开关 S2构成氢氧燃料电池,C2 附近有氧气,是电池正极,电极反应为O2+ 4H++ 4e― = 2H2O。


科目:高中化学 来源: 题型:
【题目】下列混合溶液中,各离子浓度的大小顺序正确的是( )
A.10 mL 0.1 mol/L氨水与10 mL 0.1 mol/L盐酸混合:c(Cl﹣>c(NH ![]() )>c(OH﹣)>c(H+)
)>c(OH﹣)>c(H+)
B.10 mL 0.1 mol/L NH4Cl溶液与5mL 0.2 mol/L NaOH溶液混合:c(Na+)=c(Cl﹣)>c(OH﹣)>c(H+)
C.10 mL 0.1 mol/L CH3COOH溶液与5 mL 0.2 mol/L NaOH溶液混合:c(Na+)=c(CH3COO﹣)>c(OH﹣)>c(H+)
D.10 mL 0.5 mol/L CH3COONa溶液与6 mL 1 mol/L盐酸混合:c(Cl﹣)>c(Na+)>c(OH﹣)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】广东正在建设成为海洋强省。下列说法不正确的是( )
A.从海带中提取碘单质的过程涉及氧化还原反应
B.往淡水中加入NaCl等配成人造海水,可用于海产品的长途运输
C.赤潮主要是由工农业生产和生活废水引起沿海水域的富营养化而造成的
D.海洋经济专属区的资源开发可获得Fe、Co、K Au、Mg、B等金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银锌电池是一种常见化学电源,其反应原理:Zn+Ag2O+H2O===Zn(OH)2+2Ag,其工作示意图如下。下列说法不正确的
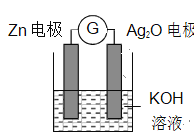
A. K+向正极移动
B. Ag2O 电极发生还原反应
C. Zn 电极的电极反应式:Zn-2eˉ+2OHˉ===Zn(OH)2
D. 放电前后电解质溶液的碱性保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A(g)+B(g)=3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A. v(A)=0.5mol·(L· s)-1 B. v(B)=0.3 mol·(L· s)-1
C. v(C)=0.8 mol·(L· s)-1 D. v(D)=1 mol·(L· s)-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的是( ) 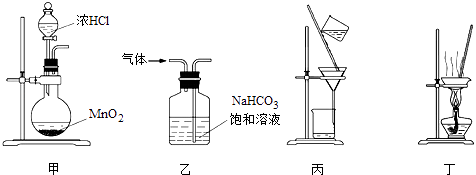
A.用装置甲制取氯气
B.用装置乙除去氯气中混有的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制MnCl24H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应最终一定有+3价铁生成的是( )
①过量的Fe与![]() 反应 ②Fe与过量稀硫酸反应后,再向其中加
反应 ②Fe与过量稀硫酸反应后,再向其中加![]() ③
③![]() 溶液中加少量盐酸 ④把Fe和
溶液中加少量盐酸 ④把Fe和![]() 的混合物溶于盐酸中
的混合物溶于盐酸中
A.只有① B.只有①② C.只有①②③ D.全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com