
下列是以芳香烃A为原料制备扁桃酸(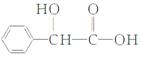 )的流程图。请回答下列问题:
)的流程图。请回答下列问题:
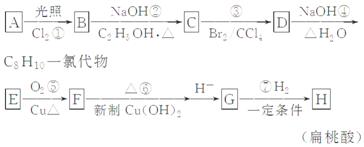
(1)A的结构简式为________,D中官能团的名称是________。
(2)C中所有碳原子________(填“能”或“不能”)共面,产物B的结构简式可能有两种,分别为________。
(3)写出下列反应的化学方程式:
E→F:________________________________________________________;
G→H:_______________________________________________________。
(4)上述转换中属于加成反应的是________(填序号)。
(5)设计实验证明物质B含有氯元素________________________________
______________________________________________________________。
【解析】 在整个转化过程中,碳链没有发生变化,因此根据扁桃酸H的结构简式确定A为乙苯,乙苯与氯气在光照条件下发生取代反应,生成一氯代物B,氯原子取代的位置不同,将有两种不同的结构
(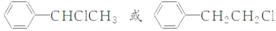 ),B中的氯原子可以用氢氧化钠的水溶液加热,发生水解反应得到氯离子,用银离子检验氯离子的存在,进而确定B中含有氯元素。在氢氧化钠的醇溶液中B发生消去反应,生成苯乙烯C,根据苯环的平面结构和乙烯的平面结构确定,有可能苯乙烯中所有的原子均在同一平面上,C中含有碳碳双键,与溴的四氯化碳溶液发生加成反应生成D(
),B中的氯原子可以用氢氧化钠的水溶液加热,发生水解反应得到氯离子,用银离子检验氯离子的存在,进而确定B中含有氯元素。在氢氧化钠的醇溶液中B发生消去反应,生成苯乙烯C,根据苯环的平面结构和乙烯的平面结构确定,有可能苯乙烯中所有的原子均在同一平面上,C中含有碳碳双键,与溴的四氯化碳溶液发生加成反应生成D( ),D在氢氧化钠的水溶液中发生取代反应引入羟基生成E(
),D在氢氧化钠的水溶液中发生取代反应引入羟基生成E( ),E经氧化得到F(
),E经氧化得到F(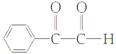 ),再次氧化得到G(
),再次氧化得到G(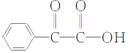 ),G与氢气发生加成反应得到扁桃酸H(
),G与氢气发生加成反应得到扁桃酸H( )。
)。

(4)③⑦
(5)取适量的物质B与NaOH水溶液混合加热,待反应完全后冷却混合溶液至室温,先后加入稍过量的HNO3溶液、AgNO3溶液,如果有白色沉淀析出则证明B中有氯元素


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
肯定属于同族元素且性质相似的是:( )
A.原子核外电子排布式:A为1s22s2,B为1s2
B.结构示意图:A为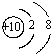 ,B为
,B为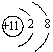
C.A原子基态时2p轨道上有1个未成对电子,B原子基态时3p轨道上也有1个未成对电子
D.A原子基态时2p轨道上有一对成对电子,B原子基态时3p轨道上也有一对成对电子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.羟基跟链烃基直接相连的化合物属于醇类
B.分子中含有羟基的化合物属于醇类
C.酚类和醇类具有相同的官能团,因而具有相同的化学性质
D.分子内含有苯环和羟基的化合物都属于酚类
查看答案和解析>>
科目:高中化学 来源: 题型:
法林是一种治疗心脑血管疾病的药物,可由化合物E和M在一定条件下合成得到(部分反应条件略)。

(1)A的名称为________,A→B的反应类型为________。
(2)D→E的反应中,加入的化合物X与新制Cu(OH)2反应产生红色沉淀的化学方程式为________________________________________________________
______________________________________________________________。
(3)G→J为取代反应,其另一产物分子中的官能团是________。
(4)L的同分异构体Q是芳香酸,Q R(C8H7O2Cl)
R(C8H7O2Cl) S
S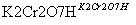 T,T的核磁共振氢谱只有两组峰,Q的结构简式为________,R→S的化学方程式为_______________________________________________________________。
T,T的核磁共振氢谱只有两组峰,Q的结构简式为________,R→S的化学方程式为_______________________________________________________________。
(5)上图中,能缩合成体型高分子化合物的酚类单体是_________________
______________________________________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.Na、Al、Fe金属单质在一定条件下与水反应都生成H2和对应的碱
B.漂白粉和明矾都常用于自来水的处理,二者的作用原理不相同
C.将SO2通入Ca(ClO)2溶液可生成CaSO3沉淀
D.过量的铜与浓硝酸反应,生成的气体只有NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
高炉炼铁是冶炼铁的主要方法,发生的主要反应为:Fe2O3(s)+3CO(g)2Fe(s)+3CO2(g)
ΔH=a kJ·mol-1。
(1)已知:①Fe2O3(s)+3C(s,石墨)===2Fe(s)+3CO(g)
ΔH1=+489.0 kJ·mol-1;
②C(s,石墨)+CO2(g)===2CO(g) ΔH2=+172.5 kJ·mol-1。则a=________。
(2)冶炼铁反应的平衡常数表达式K=________,温度升高后,K值________(填“增大”、“不变”或“减小”)。
(3)在T ℃时,该反应的平衡常数K=64,在2 L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
①甲容器中CO的平衡转化率为________。
②下列说法正确的是________(填字母)。
a.若容器内气体密度恒定时,标志反应达到平衡状态
b.增加Fe2O3的量,可以提高CO的转化率
c.甲容器中CO的平衡转化率大于乙的平衡转化率
d.甲、乙容器中,CO的平衡浓度之比为2∶3
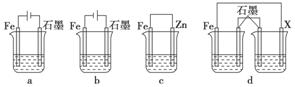
(4)采取一定措施可防止钢铁腐蚀。下列装置中的烧杯里均盛有等浓度、等体积的NaCl溶液。
①在a、b、c装置中能保护铁的是________(填字母)。
②若用d装置保护铁,X极的电极材料应是________(填名称)。
(5)25 ℃时有关物质的溶度积如下:Ksp[Mg(OH)2]=5.61×10-12,Ksp[Fe(OH)3]=2.64×10-39。25 ℃时,向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+)∶c(Fe3+)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能够成功的是 ( )
A. 只用溴水一种试剂可鉴别甲苯、己烯、乙醇、四氯化碳四种液体
B. 用苯和溴水在Fe催化下可制的溴苯
C. 用乙醇、冰醋酸和pH=1的H2SO4溶液混合加热可制备乙酸乙酯
D. 用酚酞可鉴别苯酚钠和乙酸钠两种溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有说法不正确的是
A.离子晶体的晶格能是气态离子形成1mol晶胞时放出的能量
B.金属的六方最密堆积和面心立方最密堆积的空间利用率最高
C.钠晶胞结构如右图,钠晶胞中每个钠原子的配位数为8
D.温度升高,金属的导电性将变小

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com