
����Ŀ���������(SiHCl3)���Ʊ����顢�ྦྷ�����Ҫԭ�ϣ��ش��������⣺
(1)SiHCl3�ڴ��������·�����Ӧ:
2SiHCl3(g) = SiH2Cl2(g) +SiCl4(g) ��H1 = +48kJ/mol
4SiHCl3(g) = SiH4(g) + 3SiCl4(g) ��H3 = +114kJ/mol
��Ӧ3SiH2Cl2(g) = SiH4(g) + 2SiHCl3(g)�ġ�H=______________kJ/mol��
(2)���ڷ�Ӧ2SiHCl3(g) = SiH2Cl2(g) +SiCl4(g)�����ú��ʵĴ�������323 K��343 KʱSiHCl3��ת������ʱ��仯�Ľ����ͼ��ʾ��
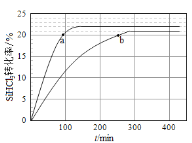
��323 Kʱ��Ӧ��ƽ��ת���ʨ� =______%���Ƚ�a��b����Ӧ���ʴ�С����a_____��b(�>������<������=��)
����343 K�£�Ҫ���SiHCl3ƽ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��_______��Ҫ���̷�Ӧ�ﵽƽ���ʱ�䣬�ɲ�ȡ�Ĵ�ʩ��_______��(���ʾ�������ѡ����ѡ����ʵ�ѡ�����)
A������Ӧ��Ũ��
B������ѹǿ
C����ʱ���������ϵ����
D��ʹ�ø���Ч�Ĵ���
��ij�¶�(T K)�£��÷�Ӧ��ʹSiHCl3��ƽ��ת���ʴﵽ30%������¶��µ�ƽ�ⳣ��KT K___K343 K(�>������<������=��)����֪��Ӧ���ʦ�=����-����=k��x2(SiHCl3)-k��x(SiH2Cl2)x(SiCl4)��k����k���ֱ�Ϊ��������Ӧ���ʳ�����xΪ���ʵ��������������ڸ��¶��µ�ת����Ϊ20%��ʱ�̣�����/����=_____________(����1λС��)��
���𰸡�-30 21 > C ABD > 2.9
��������
���ݸ�˹���ɼӼ��Ȼ�ѧ����ʽ���ۺϷ�������Է�Ӧ���ʺͻ�ѧƽ���Ӱ�죬ѧϰ���ʷ��̲�������¡����⡣
(1)Ӧ�ø�˹���ɣ�����Ӧ����֪��Ӧ�Ĺ�ϵΪ������ʽ��ǰʽ��3������H����H2����H1��3����30 kJ/mol��
(2)���¶�323 K�ϵͣ���ѧ��Ӧ����������ƽ��ʱ��ϳ���Ӧ��b���������ߣ�SiHCl3��ƽ��ת������ =21%�����Ƶأ��¶�343 K��a���������ߡ�a��b���㷴Ӧ��ת������ȣ�����Ӧ��Ũ����ͬ����a���¶ȸ���b�㣬ʹ��Ӧ������a>��b��
��A������Ӧ��Ũ�ȣ�����߷�Ӧ���ʣ����̴ﵽƽ���ʱ�䣻��Ӧ��������������䣬����Ӧ��Ũ���൱�ڼ�ѹ��SiHCl3ƽ��ת���ʲ��䡣
B������ѹǿ������߷�Ӧ���ʣ����̴ﵽƽ���ʱ�䣻��ƽ�ⲻ�ƶ���SiHCl3ƽ��ת���ʲ��䡣
C����ʱ���������ϵ���룬��Ӱ������Ӧ���ʣ���ƽ������ʹSiHCl3ƽ��ת��������
D������Ч�Ĵ���������߷�Ӧ���ʣ����̴ﵽƽ���ʱ�䣻����������ʹƽ���ƶ������ܸı�SiHCl3ƽ��ת������
���ϣ�Ҫ���SiHCl3ƽ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��C��Ҫ���̷�Ӧ�ﵽƽ���ʱ�䣬�ɲ�ȡ�Ĵ�ʩ��ABD��
����һ�գ�ͼ��343 KʱSiHCl3��ƽ��ת����Ϊ22%����֪�¶�(T K)ʱSiHCl3��ƽ��ת����30%������343 K��T K��ƽ�����ƣ�ƽ�ⳣ��KT K>K343 K��
�ڶ��գ� T Kʱ�� 2SiHCl3(g) = SiH2Cl2(g) + SiCl4(g)
������ʼʱ/mol�� 1 0 0
ת��20%ʱ/mol�� 0.8 0.1 0.1
ת��30%ʱ(ƽ��)/mol��0.7 0.15 0.15
��ѧƽ��ʱ��������������k��x2(SiHCl3)��k��x(SiH2Cl2)��x(SiCl4)�����k��/k����x(SiH2Cl2)��x(SiCl4)/x2(SiHCl3)��0.152/0.72��0.046�����¶��µ�SiHCl3��ת����Ϊ20%ʱ��������k��x2(SiHCl3)������=k��x(SiH2Cl2)��x(SiCl4)��������/����=(k��/k��)��{x2(SiHCl3)/[x(SiH2Cl2)��x(SiCl4)]}��0.046��0.82/0.12��2.9 ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��298Kʱ����0.1000mol/L NaOH��Һ�ζ�20.00mLͬŨ�ȵļ�����Һ��������ҺpH��NaOH��Һ����Ĺ�ϵ��ͼ��ʾ(��֪��HCOOH��Һ��Ka=l.0��10-4.0)
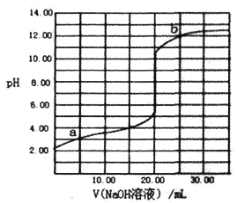
�����й�������ȷ����
A. �õζ�����Ӧ��ѡ�������Ϊָʾ��
B. ͼ��a��b�����ĵ���̶ȣ�b>a
C. ������10.00mL NaOH��Һʱ����Һ�У�c(HCOO)>c(H+)>c(Na+)>c(OH)
D. ������20.00mL NaOH��Һʱ����ҺpH>8.0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ļ������ڹ�ũҵ�����������о�����ҪӦ�á���ش��������⣺
(1)���������г���N2H4��Ϊ����������ȼ����N2H4�백�����ƣ���һ�ּ������壬������ˮ����������N2H4��H2O���õ��뷽��ʽ��ʾN2H4��H2O�Լ��Ե�ԭ���ǣ�____________________________________________��
(2)�ں��������£�1 mol NO2������C������Ӧ2NO2(g)+2C(s)![]() N2(g)+2CO2(g)�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
N2(g)+2CO2(g)�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
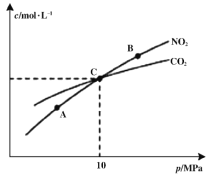
��A��B�����Ũ��ƽ�ⳣ����ϵ��Kc(A) ___________Kc(B)(�<����>����=��)
��A��B��C������NO2��ת������ߵ���___________(�A����B����C��)�㡣
������C��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��Kp=___________MPa(Kp����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
(3)��֪��������(HNO2)���ʺ��������ƣ�������һ�����ᡣ������������ĵ���ƽ�ⳣ��Ka=5.1��10��4��H2CO3��Ka1=4.2��10��7��Ka2=5.61��10��11���ڳ���������2mol̼���Ƶ���Һ�м���1mol��HNO2������Һ��CO32����HCO3����NO2��������Ũ���ɴ�С��˳����______________________��
(4)��֪�������¼װ�(CH3NH2)�ĵ��볣��ΪKb����pKb=��lgKb=3.4ˮ��Һ����CH3NH2+H2OCH3NH3++OH������������CH3NH2��Һ�μ�ϡ������c(CH3NH2)=c(CH3NH3+)ʱ������ҺpH=_______��
(5)һ��ú̿������������Ԫ����CaSO4���γɹ̶���������������CO�ֻ���CaSO4������ѧ��Ӧ����ص��Ȼ�ѧ����ʽ���£�
��CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) ��H=+210.5kJ�� mol��1
��CaSO4(s)+4CO(g) CaS(s)+ 4CO2(g) ��H=��189.2 kJ�� mol��1
��ӦCaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g) ��H=___________ kJ�� mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019 ���ǡ����ʻ�ѧԪ�����ڱ��ꡱ�� 1869 ���Ž��з�ѵ�ʱ��֪��Ԫ�ظ�����������ѧ���ʽ������У�ȷԤ���˼ס�������δ֪Ԫ�ص�λ�ã���Ԥ���˶��ߵ����ԭ������������ԭʼ��¼���¡�����˵���д������

A. ��λ������Ԫ�����ڱ��������ڵڢ�A ��B. ԭ�Ӱ뾶�Ƚϣ��ף��ң� Si
C. �ҵļ���̬�⻯����ȶ���ǿ��CH4D. �Ʋ��ҵĵ��ʿ��������뵼�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�������õ����ʵ����ķ�Ӧ���ں���������ģ�ҵ����SO3���õ�����ʵ���������±���ʾ��
ʵ�� ��� | �¶� ������ | SO2Ũ�ȣ�mo1/L�� | ||||||
0min | 10min | 20min | 30min | 40min | 50min | 60min | ||
1 | 300 | 2.00 | 1.70 | 1.50 | 1.36 | 1.25 | 1.20 | 1.20 |
2 | 300 | 2.00 | 1.50 | 1.28 | 1.20 | 1.20 | 1.20 | 1.20 |
3 | 500 | 2.00 | 1.60 | 1.39 | 1.29 | 1.27 | 1.27 | 1.27 |
��1��ʵ��1�У�50��60mnʱ��Σ�SO2Ũ�Ⱦ�Ϊ1.20mo1/L��ԭ����___��
��2��ʵ��2�У�ǰ20min����O2��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧ����Ϊ___��
��3������ʵ���У�ֻ��1��2�е�ij��ʹ���˴�������ʹ�ô�����Ϊ��___�飬����ʵ��1��2�е����ݣ�����Ϊ����___�����������������������ı�SO2��ƽ��ת���ʣ�������___��
��4�����������е����ݣ��¶����ߣ�SO2��ƽ��ת���ʻ�___��������������������������С������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ��2H2O(l)![]() 2H2(g)+O2(g)+Q1�ͷ�Ӧ��2H2O(l)
2H2(g)+O2(g)+Q1�ͷ�Ӧ��2H2O(l)![]() 2H2(g)+O2(g)+Q2�����Ƿֽ�õ�H2��O2�������жϴ�����ǣ� ��
2H2(g)+O2(g)+Q2�����Ƿֽ�õ�H2��O2�������жϴ�����ǣ� ��
A. ��Ӧ����̫����ת��Ϊ��ѧ��B. ��Ӧ���е���ת��Ϊ��ѧ��
C. Q1>0��Q2<0D. Q1=Q2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ǹ��ɿ������ʯ����Ҫ�ɷ֣����ʹ輰�仯������й㷺����;�����������գ�
��1��ijЩ�����ξ���ɸѡ���ӵĹ��ܡ�һ�ֹ����ε����Ϊ��M2O��R2O3��2SiO2��nH2O����֪Ԫ��M��R��λ��Ԫ�����ڱ��ĵ�3���ڣ���Ԫ��ԭ�ӵ�������֮��Ϊ24��
��д��Mԭ�Ӻ���������ߵĵ��ӵĵ����Ų�ʽ��___________��
�ڳ����£�������R���ʷ�����Ӧ����_______��ѡ����ţ���
a��CuCl2��Һ b��Fe2O3 c��Ũ���� d��NaOH��Һ e��Na2CO3����
��2�������裨Si3N4���մɲ���Ӳ�ȴ��۵�ߡ��������з�Ӧ�Ƶã�SiO2+C+N2![]() Si3N4+CO
Si3N4+CO
��Si3N4�е�Ԫ�صĻ��ϼ�Ϊ-3�������Si3N4�е�Ԫ�ػ��ϼ�Ϊ���۵�ԭ��__________________��
��C3N4�Ľṹ��Si3N4���ƣ���Ƚ϶����۵�ߵͣ���˵�����ɣ�______________________��
����ƽ������Ӧ�Ļ�ѧ����ʽ�����������ת�Ƶ���Ŀ�ͷ���_______________��
��3��һ���ù�ҵ�裨����������ͭ�Ƚ�����������Ʊ�Si3N4����Ҫ�������£�
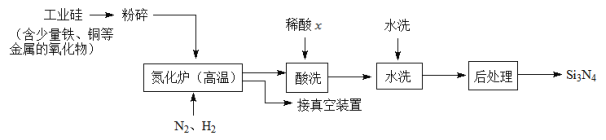
�ٽ���ҵ������Ŀ����______________________________��
��������H2��Ϊ���ž��豸�еĿ�������H2�ڸ�����Ҳ�ܻ�ԭ��ҵ���е�ijЩ�������![]() ������______��ѡ������ᡱ�����ᡱ�����ᡱ����������_____________________��
������______��ѡ������ᡱ�����ᡱ�����ᡱ����������_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͭ(Cu2O)��һ����;�㷺�Ĺ����ϣ�ij��������ͭ��ʯ(�� CuFeS2��Cu2S��)Ϊԭ����ȡCu2O�Ĺ����������£�
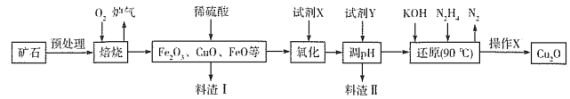
�����¼������ʿ�ʼ�γɳ�������ȫ����ʱ��pH���±�

(1)¯���е��к�����ɷ���___________��Cu2S��O2��Ӧʱ���������뻹ԭ�������ʵ���֮��Ϊ___________��
(2)���Լ�X��H2O2��Һ��д����Ӧ��Ӧ�����ӷ���ʽ��______________________�����Լ�X��___________ʱ���������ڽ��������ɱ���
(3)�����Լ�Y��pHʱ��pH�ĵ��ط�Χ��______________________��
(4)д����N2H4�Ʊ�Cu2O�Ļ�ѧ����ʽ��______________________������X����___________��ϴ�ӡ���ɣ����к��ʱҪ������������Ŀ����___________��
(5)��ͭ��ʯī���缫�����Ũ��ǿ������Һ���Ƶ�����Cu2O��д������������Cu2O�ĵ缫��Ӧʽ��_________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʵıȽ��У�����ȷ����
A. Ӳ���ɴ�С�����ʯ��̼���裾�����
B. �����ܣ�NaBr<NaCl<MgO
C. ���ļ��ԣ�N��H<O��H<F��H
D. �۵㣺![]()
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com